题目内容
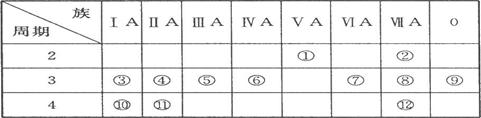
(9分)下表是周期表的一部分,试回答下列问题
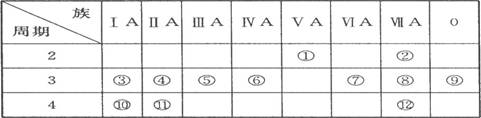
(1)、表中元素中,第一电离能最小的元素是 (填元素符号,下同),电负性最大的元素是 ,单质中化学性质最不活泼的是__________ (填化学式)。
(2)、表中元素的最高价氧化物对应水化物中,酸性最强的是 (填化学式,下同),碱性最强的是 ,呈两性的氢氧化物是 。
(3)、表中ⅦA元素中最不稳定的氢化物是__________(填化学式)。
(4)、为什么表中的④第一电离能比⑤大?
______________________________________________ 。
【答案】
(1)、K、F、Ar(各1分); (2)、HClO4、KOH、Al(OH)3 (各1分)
(3)、HBr(1分); (4)、镁的外围电子为3S2,处于全满状态,是相对稳定结构。(2分)
【解析】(1)金属性越强,第一电离能越小;非金属性越强电负性越大,所以第一电离能最小的是K,电负性最大的是F。稀有气体的最外层电子数已经达到饱和,所以性质最不活泼。
(2)非金属性越强,最高价氧化物的水化物的酸性越强,同样金属性越强,最高价氧化物的水化物的碱性越强,因此分别是HClO4、KOH。两性氢氧化物是Al(OH)3 。
(3)非金属性越弱,相应氢化物的稳定性越弱,因此是HBr。
(4)由于镁原子的3s轨道电子是全充满状态,所以稳定性强,第一电离能大于铝的。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
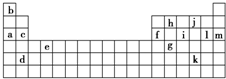
下表是周期表的一部分,表中所列的字母分别代表某一化学元素。
| b | | | |||||||||||||||
| | | | | h | | j | | | |||||||||
| a | c | f | | i | | l | m | ||||||||||
| | | | e | | | | | | | | | | g | | k | | |
| | d | | | | | | | | | | | | | | | | |
(2) 将元素a、c、d、f、l、b的原子半径按由大到小的顺序排列________________________。
(3) i元素属于_______________(填金属或非金属)元素,它的最高化合价是____________,
最低化合价是___________。它能与氧气反应,生成一种吸水性很强的物质,这种物质在实验室里常用做干燥剂,写出i的单质与氧气反应的化学方程式:_________________
 下表是周期表的一部分,表中所列的字母分别代表某一化学元素.
下表是周期表的一部分,表中所列的字母分别代表某一化学元素.