题目内容
下列各组溶液,只用试管和胶头滴管,不用任何试剂就可以鉴别的是( )
①稀H2SO4和Na2CO3 ②KOH和Al2(SO4)3 ③Ca(OH)2和NaHCO3 ④NaAlO2和稀盐酸.
①稀H2SO4和Na2CO3 ②KOH和Al2(SO4)3 ③Ca(OH)2和NaHCO3 ④NaAlO2和稀盐酸.
| A、①②④ | B、①②③ |
| C、①③④ | D、全部 |
考点:物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题
分析:只用试管和胶头滴管而不用其它试剂就能区分,说明反应现象与反应物的量多少有关,结合物质间的反应来分析解答.
解答:
解:①稀H2SO4和Na2CO3,当硫酸少量时,离子反应方程式为CO32-+H+=HCO3-,当硫酸过量时,离子反应方程式为2H++CO32-=CO2↑+H2O,所以反应现象不同,故正确;
②KOH和Al2(SO4)3 ,当Al2(SO4)3溶液过量时,反应离子方程式为:Al3++3OH-=Al(OH)3↓,当Al2(SO4)3少量时,离子反应方程式为Al3++4OH-=AlO2-+2H2O,所以反应现象不同,故正确;
③Ca(OH)2和NaHCO3,无论二者谁过量,都会生成碳酸钙沉淀,所以现象相同,不能鉴别,故错误;
④NaAlO2和稀盐酸,当盐酸少量时,离子反应方程式为H++AlO2-+H2O=Al(OH)3↓,当盐酸过量时,离子反应方程式为:4H++AlO2-=Al3++2H2O,所以反应现象不同,故正确;
则正确的有①②④;
故选A.
②KOH和Al2(SO4)3 ,当Al2(SO4)3溶液过量时,反应离子方程式为:Al3++3OH-=Al(OH)3↓,当Al2(SO4)3少量时,离子反应方程式为Al3++4OH-=AlO2-+2H2O,所以反应现象不同,故正确;
③Ca(OH)2和NaHCO3,无论二者谁过量,都会生成碳酸钙沉淀,所以现象相同,不能鉴别,故错误;
④NaAlO2和稀盐酸,当盐酸少量时,离子反应方程式为H++AlO2-+H2O=Al(OH)3↓,当盐酸过量时,离子反应方程式为:4H++AlO2-=Al3++2H2O,所以反应现象不同,故正确;
则正确的有①②④;
故选A.
点评:本题考查了物质间的反应,明确物质的性质是解本题关键,侧重于考查学生对基础知识的应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
如图有机物的系统命名是( )
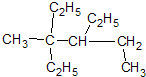

| A、2,2,3-三乙基戊烷 |
| B、3-甲基-3,4-二乙基己烷 |
| C、1-甲基-2,3,3-三乙基丁烷 |
| D、4-甲基-3,4-二乙基己烷 |
下列各组变化中,前者是物理变化,后者是化学变化的是( )
| A、煤的气化、煤的干馏 |
| B、用盐酸除金属表面的锈、食盐水导电 |
| C、焰色反应、石油的裂化 |
| D、热的饱和KNO3溶液降温析出晶体、二硫化碳洗涤试管内壁上的硫 |
下列离子方程式书写正确的是( )
A、用惰性电极电解饱和MgCl2溶液:2Cl-+2H2O
| ||||
| B、将标准状况下112 mL氯气通入10 mL 1 mol?L-1的溴化亚铁溶液中:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 | ||||
| C、NaHSO4溶液与Ba(OH)2溶液混合后溶液呈中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | ||||
| D、向澄清石灰水中加入过量的碳酸氢钠溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O |
短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是其内层电子总数的3倍,Y原子最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列叙述错误的是( )
| A、原子半径的大小顺序:Y>Z>W>X |
| B、元素W的最高价氧化物对应水化物的酸性比Z的强 |
| C、元素X的两种氢化物中,常温常压下均为液态,有一种含氢键,另一种没有氢键 |
| D、化合物YX、ZX2的化学键类型不相同 |
常温下,下列各组离子在指定溶液中能大量共存的是( )
| A、c(H+)/c(OH-)=1012的水溶液中:NH4+、Al3+、NO3-、Cl- |
| B、水电离出的c(H+)=10-12mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| C、pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ |
| D、c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、SO42-、SCN- |
下列物质不能为动物体提供能量的是( )
| A、脂肪 | B、维生素 |
| C、糖类 | D、蛋白质 |
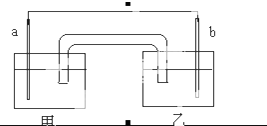 某化学兴趣小组设计如图原电池:其中a、b分别为Cu和Ag,甲和乙分别是氨水和硝酸银溶液,盐桥的琼脂中吸附有KCl溶液,反应一段时间后,下列说法正确的是( )
某化学兴趣小组设计如图原电池:其中a、b分别为Cu和Ag,甲和乙分别是氨水和硝酸银溶液,盐桥的琼脂中吸附有KCl溶液,反应一段时间后,下列说法正确的是( )| A、b为负极,电极方程式为:Ag++e-═Ag |
| B、甲中出现大量蓝色沉淀 |
| C、总反应为:Cu+2Ag+═Cu2++Ag |
| D、反应时,盐桥中的K+向乙方向移动 |
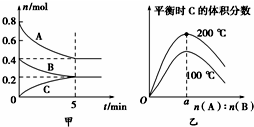 在2L的密闭容器中发生反应xA(g)+yB(g)?zC(g).图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是( )
在2L的密闭容器中发生反应xA(g)+yB(g)?zC(g).图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是( )| A、200℃时,反应从开始到平衡的平均速率v(B)=0.04 mol?L-1?min-1 |
| B、200℃时,该反应的平衡常数为25 L2/mol2 |
| C、当外界条件由200℃降温到100℃,原平衡一定被破坏,且正逆反应速率均增大 |
| D、由图乙可知,反应xA(g)+yB(g)?zC(g)的△H<0,且a=2 |