题目内容
7.下列各表述与示意图一致的是( )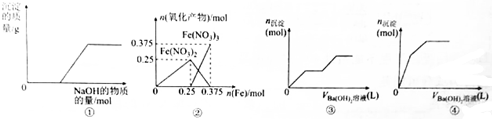
| A. | 图①表示向Ca(HCO3)2溶液中滴加NaOH溶液时,产生沉淀的质量与加入NaOH的物质的量之间的关系 | |
| B. | 图②表示向n(HNO3)=1mol的稀HNO3中加入Fe时,氧化产物(还原产物为NO)的物质的量与Fe的物质的量之间的关系 | |
| C. | 图③可用来表示向含有4mol HCl和1mol MgSO4的混合溶液中滴加Ba(OH)2溶液时,产生沉淀的物质的量(n)与加入Ba(OH)2溶液体积(V)之间的关系 | |
| D. | 图④表示向一定质量的明矾溶液中滴加Ba(OH)2溶液时,产生沉淀的物质的量(n)与加入Ba(OH)2溶液体积(V)之间的关系 |
分析 A.Ca(HCO3)2溶液中滴加NaOH溶液,开始即生成沉淀;
B.稀HNO3中加入Fe时,开始先生成3Fe(NO3)3,Fe过量生成3Fe(NO3)2;
C.向含有4mol HCl和1mol MgSO4的混合溶液中滴加Ba(OH)2溶液时,先产生的沉淀只是BaSO4,然后是中和反应,最后是与Mg2+产生沉淀Mg(OH)2;
D.先发生的反应是2KAl(SO4)2+3Ba(OH)2=2Al(OH)3↓+3BaSO4↓+K2SO4,然后2Al(OH)3+K2SO4+Ba(OH)2=2KAlO2+BaSO4↓+H2O,即沉淀达最多后溶解一部分(5mol→4mol).
解答 解:A.Ca(HCO3)2溶液中滴加NaOH溶液,开始即生成沉淀,图象中开始没有沉淀,故A错误;
B.稀HNO3中加入Fe时,开始先生成3Fe(NO3)3,Fe过量生成3Fe(NO3)2,发生反应为Fe+4HNO3(稀)═Fe(NO3)3+NO↑+2H2O,2Fe(NO3)3+Fe═3Fe(NO3)2,图象不符,故B错误;
C.向含有4mol HCl和1mol MgSO4的混合溶液中滴加Ba(OH)2溶液时,先发生酸碱中和反应,然后是中和反应,最后是与Mg2+产生沉淀Mg(OH)2,故C正确;
D.向一定质量的明矾溶液中滴加Ba(OH)2溶液时,先发生的反应是2KAl(SO4)2+3Ba(OH)2=2Al(OH)3↓+3BaSO4↓+K2SO4,然后2Al(OH)3+K2SO4+Ba(OH)2=2KAlO2+BaSO4↓+H2O,即沉淀达最多后溶解一部分(5mol→4mol),即图象中沉淀的量先增多,后减少,最后不变,故D错误;
故选C.
点评 本题考查物质之间的反应,明确离子反应先后顺序是解本题关键,侧重于考查学生的分析能力和读图能力,题目难度中等.

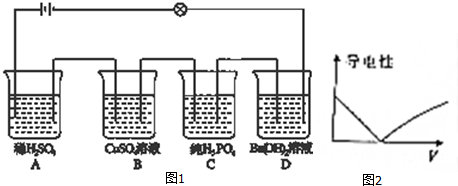
(1)上述实验中发生的反应有Zn+Cu2+=Zn2++Cu、Zn+2H+=Zn2++H2↑.(离子方程式)
(2)硫酸铜溶液可以加快氢气生成速率的原因是通过一系列反应构成了原电池,写出该原电池的电极反应式,负极:Zn-2e-=Zn2+;正极:2H++2e-=H2↑.
(3)要加快上述实验中气体产生的速率,还可采取的措施有BC.
A.将稀硫酸换成浓硫酸 B.适当升高温度
C.用锌粉代替锌粒 D.增加上述稀硫酸的用量
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因当加入一定量的硫酸铜后,生成的单质铜会沉积在锌的表面,降低了锌与溶液的接触面积.
| 选项 | 物质 | 用途 | 解释 |
| A | Al2O3 | 耐火材料 | Al2O3的熔沸点较高 |
| B | SiO2 | 计算机芯片 | SiO2是一种良好的半导体 |
| C | Fe3O4 | 红色涂料 | Fe3O4是一种红色氧化物 |
| D | 浓H2SO4 | 干燥剂 | 浓H2SO4有脱水性 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 过滤 | B. | 溶解 | C. | 蒸发 | D. | 分液 |
| A. | 氯化钡 | B. | 硫酸铜 | C. | 硝酸钾 | D. | 氯酸钾 |
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 反应在前50 s 的平均速率v(PCl3)=0.0032 mol•L-1•s-1 | |
| B. | 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol•L-1,则反应的H<0 | |
| C. | 相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3 和0.20 mol Cl2,反应达到平衡前 v(正)>v(逆) | |
| D. | 相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,PCl3 的转化率小于80% |