题目内容
17.刘禹锡的“千淘万漉虽辛苦,吹尽狂砂始到金”,这首诗句反映了对淘金过程的描写,下列说法中正确的是( )| A. | “千淘万漉”的基本原理是化学中的萃取 | |
| B. | 24K金(纯金)的各方面物理性能都比18K金优越 | |
| C. | 在铜件外镀金,金镀层破损了,会加快铜件的腐蚀速率 | |
| D. | 常温下,金不易被氧化,不与其它任何物质发生化学反应 |
分析 沙里淘金是利用黄金和沙子的密度的不同,用水洗的方法将沙子和黄金分离;金不如铜活泼,故铜件外镀金后,一旦金属镀层破损,则形成原电池,铜做负极,金做正极,据此分析.
解答 解:A、沙里淘金是利用黄金和沙子的密度的不同,用水洗的方法将沙子和黄金分离,不是萃取,故A错误;
B、纯金较软,故并不是各方面的物理性能都比18K金优越,故B错误;
C、金不如铜活泼,故铜件外镀金后,一旦金属镀层破损,则形成原电池,铜做负极,金做正极,故能加快铜件的腐蚀,故C正确;
D、金是较稳定的金属,但并不意味着在常温下和任何物质均不反应,金在常温下溶于王水,故D错误.
故选C.
点评 本题借助文言文考查了金的物理性质和化学性质,应注意的是金能溶于王水.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
11.如图是部分短周期主族元素原子半径与原子序数的关系.下列说法正确的是( )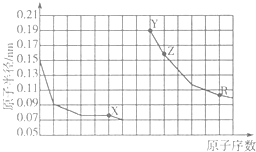

| A. | X、R的最简单氢化物的稳定性:X<R | |
| B. | X、Y、Z形成简单离子的半径大小:X>Y>Z | |
| C. | X、Y形成的化合物中只含有离子键 | |
| D. | Z单质着火可以用干冰进行灭火 |
8.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1.8g H218O中含有的中子数为NA | |
| B. | 1mol Fe与足量的浓硫酸反应,生成SO2的分子数为NA | |
| C. | 7.1g Cl2溶于水所得溶液中含有的Cl-数目为0.1NA | |
| D. | 丙烷燃料电池负极消耗2.24L(标准状况)气体时,电路中转移电子数为2NA |
2.高温下,2.8g铁粉与水蒸气反应,向反应后所得固体物中加入足量硝酸,得到NO和NO2混合气体1.008L(标准状况),则反应后所得固体物中未参加反应的铁可能是( )
| A. | 0.595g | B. | 1.42g | C. | 2.485g | D. | 2.72g |
9.如图甲是利用一种微生物将废水中的尿素[CO(NH2)2]的化学能直接转化为电能,并生成环境友好物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中不正确的是( )

| A. | 铜电极应与X相连接 | |
| B. | H+透过质子交换膜由左向右移动 | |
| C. | M电极反应式为CO(NH2)2+H2O-6e-═CO2↑+N2↑+6H+ | |
| D. | 当N电极消耗0.25 mol气体时,则理论上铁电极增重32 g |
6.下列说法正确的是( )
| A. | 某温度下水的离子积常数为Kw,在该温度下,a mol•L-1一元酸HA与b mol•L-1一元碱BOH等体积混合,溶液呈中性,则溶液中c(H+)=$\sqrt{Kw}$ | |
| B. | 已知MgCO3的Ksp=6.82×10-6mol2•L-2,则在含有固体MgCO3的Na2CO3溶液中,有c(Mg2+)=c(CO32-),且c(Mg2+)•c(CO32-)=6.82×10-6mol2•L-2 | |
| C. | Ksp(AB2)小于Ksp(CD),说明AB2的溶解度小于CD的溶解度 | |
| D. | NH4Cl和NH3•H2O的混合溶液中,分别存在NH4+的水解平衡和NH3•H2O的电离平衡,二者对对方的平衡都起了促进作用 |
7.某同学在实验室探究NaHCO3的性质:常温下,配制0.10mol/LNaHCO3溶液,测其pH为8.4;取少量该溶液滴加CaCl2溶液至pH=7,滴加过程中产生白色沉淀,但无气体放出.下列说法不正确的是( )
| A. | NaHCO3溶液呈碱性的原因是HCO3-的水解程度大于电离程度 | |
| B. | 加入CaCl2促进了HCO3-的电离 | |
| C. | 反应的离子方程式是2HCO3-+Ca2+═CaCO3↓+H2CO3 | |
| D. | 反应后的溶液中存在:c(Na+)+2c(Ca2+)=c(HCO3-)+2c(CO32-)+c(Cl-)+c(H2CO3) |
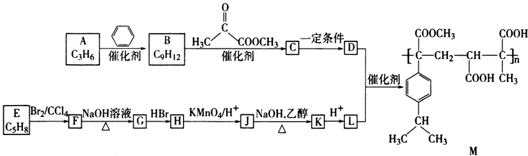
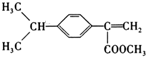 、
、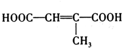 (写结构简式).
(写结构简式).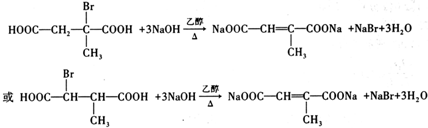 .
.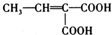 (写结构简式).
(写结构简式).