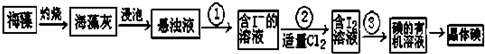
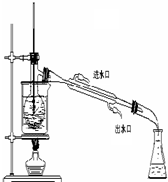
题目内容
下列反应中,氯元素被氧化的是( )
A、2KClO3
| ||||
B、2Na+Cl2
| ||||
| C、MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O | ||||
D、H2+Cl2
|
考点:氧化还原反应
专题:氧化还原反应专题
分析:Cl元素被氧化,则元素化合价应升高,以此解答.
解答:
解:A.反应中Cl元素化合价降低,被还原,故A错误;
B.反应中Cl元素化合价由0价降低到-1价,被还原,故B错误
C.Cl元素化合价由-1价升高到0价,被氧化,故C正确;
D.反应中Cl元素化合价由0价降低到-1价,被还原,故D错误.
故选C.
B.反应中Cl元素化合价由0价降低到-1价,被还原,故B错误
C.Cl元素化合价由-1价升高到0价,被氧化,故C正确;
D.反应中Cl元素化合价由0价降低到-1价,被还原,故D错误.
故选C.
点评:本题考查氧化还原反应,为高频考点,侧重于学生的分析能力的考查,从元素化合价的角度解答该题,难度不大.

练习册系列答案
相关题目
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O下列有关说法中不正确的是( )
| A、HNO3在反应中既表现氧化性也表现出酸性 |
| B、每生成22.4L NO(标准状况)有3mol电子转移 |
| C、HNO3作氧化剂,铜作还原剂,3mol Cu还原8mol的HNO3 |
| D、HNO3作氧化剂,铜作还原剂,3mol Cu还原2mol的HNO3 |
下列实验不能达到目的是( )
| A、往酸性KMnO4溶液中通入SO2验证SO2的还原性 |
| B、加热氯化铵与氢氧化钙固体混合物制取氨气 |
| C、用二氧化锰和稀盐酸反应制取氯气 |
| D、在溴水、碘水中加入四氯化碳以萃取其中的溴、碘 |
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色呈黄色.五种元素核电荷数之和为54,最外层电子数之和为20.W、Z最外层电子数相同,Z的核电荷数是W的2倍.工业上一般通过电解氧化物的方法获得Y的单质.则下列说法不正确的是( )
| A、原子半径:X>Y>Q>W |
| B、元素Y与元素Z的最高正化合价之和的数值等于8 |
| C、Q和Z所形成的化合物为共价化合物 |
| D、X、Q和W三种元素形成的化合物的水溶液呈碱性 |
全钒电池以惰性材料作电极,在电解质溶液中发生的电池总反应为:
VO2+(蓝色)+H2O+V3+(紫色)
VO2+(黄色)+V2+(绿色)+2H+
下列说法错误的是( )
VO2+(蓝色)+H2O+V3+(紫色)
| 放电 |
| 充电 |
下列说法错误的是( )
| A、充电时,阳极附近溶液由蓝色逐渐变为黄色 |
| B、放电过程中,正极附近溶液的酸性减弱 |
| C、充电时,反应每生成2mol H+时电子转移数为2mol |
| D、放电时,负极反应为V2+-e-=V3+ |
W、X、Y、Z是原子序数依次增大的四种短周期元素,化合物WX能抑制水的电离.化合物Y2Z能促进水的电离,则Y元素是( )
| A、F | B、Cl | C、Li | D、Na |
将2mol气体A和3mol气体B在一定条件下发生反应:A(g)+3B(g)?2C(g)△H<0,达到平衡时,B的转化率为50%,则A的转化率为( )
| A、17% | B、20% |
| C、25% | D、50% |