题目内容
已知
①2C(s)+O2(g)===2CO(g);ΔH=-221.0kJ·mol-1
②2H2(g)+O2(g)===2H2O(g);ΔH=-483.6kJ·mol-1
则反应C(s)+H2O(g)===CO(g)+H2(g)的ΔH为
- A.+131.3kJ·mol-1
- B.-131.3kJ·mol-1
- C.-352.3kJ·mol-1
- D.+262.6kJ·mol-1
A
试题分析:根据盖斯定律知反应(①-②)/2得目标反应,则ΔH= = 131.3kJ/mol。答案选A。
= 131.3kJ/mol。答案选A。
考点:盖斯定律
点评:不管化学反应是一步完成或分几步完成,其反应热是不变的。即化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。
试题分析:根据盖斯定律知反应(①-②)/2得目标反应,则ΔH=
 = 131.3kJ/mol。答案选A。
= 131.3kJ/mol。答案选A。考点:盖斯定律
点评:不管化学反应是一步完成或分几步完成,其反应热是不变的。即化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
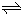
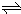 N2O4(g)△H<0,升高温度,正逆反应的速率都增大,但正反应的增速大于逆反应增速
N2O4(g)△H<0,升高温度,正逆反应的速率都增大,但正反应的增速大于逆反应增速