题目内容
7. 25℃时某些弱酸的电离平衡常数如下表所示:
25℃时某些弱酸的电离平衡常数如下表所示:| CH3COOH | HClO | H2CO3 |
| K(CH3COOH) =1.8×10-5 | K(HClO) =3.0×10-8 | K(H2CO3)a1=4.4×10-7 K(H2CO3)a2=4.7×10-11 |
| A. | 相同浓度的CH3COOH和HClO的混合溶液中,各离子浓度的大小关系是:c(H+)>c(ClO-)>c(CH3COO-)>c(OH-) | |
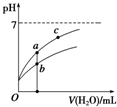
| B. | 图象中a、c两点所处的溶液中$\frac{c({R}^{-})}{c(HR)•c(O{H}^{-})}$相等(HR代表CH3COOH或HClO) | |
| C. | 图象中a点酸的浓度大于b点酸的浓度 | |
| D. | 向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O=2HClO+CO32- |
分析 A.酸的电离常数越大,则酸根离子的浓度越大;
B.在$\frac{c({R}^{-})}{c(HR)•c(O{H}^{-})}$的分子、分母同时乘以氢离子浓度可得:$\frac{K(HR)}{{K}_{w}}$,温度不变,则该比值不变;
C.先根据电离程度大小判断醋酸、次氯酸对应曲线及起始浓度大小,a、b两点加入水的体积相同,则此时酸溶液浓度取决于酸的起始浓度;
D.根据强酸制取弱酸判断,反应生成的应该为碳酸氢根离子.
解答 解:A.醋酸的电离常数大于次氯酸,所以相同浓度的CH3COOH和HClO的混合溶液中,各离子浓度的大小关系是:c(H+)>c(CH3COO-)>c(ClO-)>c(OH-),故A错误;
B.在$\frac{c({R}^{-})}{c(HR)•c(O{H}^{-})}$的分子、分母同时乘以氢离子浓度可得:$\frac{K(HR)}{{K}_{w}}$,温度不变,则该比值不变,由于水的离子积和电离平衡常数只受温度影响,a、c的温度相同,则该比值相等,故B正确;
C.pH相等的CH3COOH、HClO,稀释相同的倍数时,较强酸中氢离子浓度小于较弱酸,则较弱酸的pH小于较强酸,酸性CH3COOH>HClO,所以a所在曲线表示CH3COOH,b所在曲线表示HClO,次氯酸的电离程度小于醋酸,所以醋酸的浓度减小,次氯酸的浓度较大,a、b两点相比,加入相同体积的水后仍然是次氯酸的浓度较大,即:图象中a点酸的浓度小于b点酸的浓度,故C错误;
D.碳酸的二级电离小于次氯酸,所以碳酸氢根离子的酸性小于次氯酸,则向NaClO溶液中通入少量二氧化碳的离子方程式:ClO-+CO2+H2O═HClO+HCO3-,故D错误;
故选B.
点评 本题考查电解质的强弱与电离常数的关系,题目难度中等,试题侧重于学生的分析能力和计算能力的考查,明确酸的电离常数与酸的强弱、酸根离子水解能力的关系是解本题关键.

| A. | NaCl | B. | NaHCO3 | C. | NaHSO3 | D. | NaHS |
| A. | 氨是生产氮肥的重要原料 | |
| B. | 开发使用高效、低毒、低残留的第三代环境友好型农药 | |
| C. | 大力推广有机氯、有机磷等有机合成农药 | |
| D. | 磷肥和钾肥可从无机盐中获得 |
| A. | 氨水与盐酸反应:OH-+H+═H2O | |
| B. | 锌与硫酸铜溶液反应:Zn+Cu2+═Zn2++Cu | |
| C. | 铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 氢氧化钡与硫酸反应:Ba2++SO42-═BaSO4↓ |
| A. | 液氨受热汽化 | B. | 加热使碘化氢气体分解 | ||
| C. | 加热使金属铝熔化 | D. | 加热使硅晶体熔化 |
| A. | 铅笔芯的主要成分是金属铅 | |
| B. | CO气体有毒,在生有炉火的居室中多放几盆水,可吸收CO | |
| C. | 含磷洗衣粉的大量使用会造成水体富营养化 | |
| D. | 水泥、玻璃、塑料都是高分子材料 |
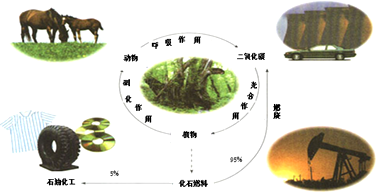
(1)有关碳循环的说法中正确的是ac
a.光合作用是光能转化成化学能b.化石燃料是可再生的
c.循环过程有氧化还原反应d.石油中含乙烯、丙烯,通过加聚反应得到高分子化合物
(2)用钌的配合物作催化剂,一定条件下可直接光催化分解CO2发生反应:2CO2(g)=2CO(g)+O2(g),该反应的△H0>,(选填:>、<、=).
(3)CO2转化途径之一是:利用太阳能或生物质能分解水制H2,然后将H2与CO2转化为甲醇或其它的物质.
2H2O(1)=2H2(g)+O2(g)△H=+571.5kJ•mol-1
3H2(g)+CO2(g)=CH3OH(l)+H2O(1)△H=-137.8kJ•mol-1
则反应:4H2O (1)+2CO2(g)=2CH3OH(l)+3O2(g)△H=kJ•mol-1.
你认为该方法需要解决的技术问题有:.
a.开发高效光催化剂
b.将光催化制取的氢气从反应体系中有效分离,并与CO2催化转化.
c.二氧化碳及水资源的来源供应
(4)用稀氨水喷雾捕集CO2最终可得产品NH4HCO3.在捕集时,气相中有中间体NH2COONH4(氨基甲酸铵)生成.现将一定量纯净的氨基甲酸铵置于恒容的密闭真空容器中,分别在不同温度下进行反应:NH2COONH4(s)?2NH3(g)+CO2(g).实验测得的有关数据见下表.( t1<t2<t3)
| 温度(℃) 气体总浓度 (mol/L) 时间(min) | 15 | 25 | 35 |
| 0 | 0 | 0 | 0 |
| t1 | 9×10-3 | 2.7×10-2 | 8.1×10-2 |
| t2 | 3×10-2 | 4.8×10-2 | 9.4×10-2 |
| t3 | 3×10-2 | 4.8×10-2 | 9.4×10-2 |
(5)用一种钾盐水溶液作电解质,CO2电催化还原为碳氢化合物(其原理见图).在阴极上产生乙烯的电极反应方程式为:2CO2+12H++12e-=CH2=CH2+4H2O.
