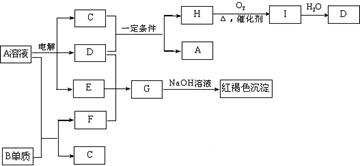
题目内容
(08安师大附中二模)工业上用饱和食盐水作原料,用电解方法制取烧碱。
(1)写出电极反应和总化学方程式:阳极______________________,阴极_________________________;总反应________________________。
(2)NaOH在_________极附近生成;
(3)电极材料为石墨和铁网,阳极必须用_________,原因是
___________________________________________;
(4)电解过程中可能发生的副反应有两个,它们是:
______________________________________,
(5)若将电解槽内的隔膜去掉,同时升高电解液的温度,此时电解产物间发生反应:NaOH+Cl2→NaClO3+NaC1+H2O(未配平),假设反应进行完全,则在该条件下最后得到的两种产物的物质的量之比是______________
(6)若在NaClO3溶液中加入固体KCl,则可得到重要工业产品KClO3晶体,其原因是_______________________________________________。
答案:(1)2Cl--2e==Cl2 2H+2e==H2 2NaCI+2H2O  2NaOH+H2+O2
2NaOH+H2+O2
(2)阴
(3)石墨;因为阳极发生氧化反应故必须用惰性电极
(4)2NaOH+Cl2===NaCl+NaClO+H2O O2+H2O===HCl+NaClO
(5)n(NaClO3):n(H2)==1:3
(6)KClO3溶解度比NaClO3小
(2)阴
(3)石墨;因为阳极发生氧化反应故必须用惰性电极
(4)2NaOH+Cl2===NaCl+NaClO+H2O O2+H2O===HCl+NaClO
(5)n(NaClO3):n(H2)==1:3
(6)KClO3溶解度比NaClO3小

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目