题目内容
下列物质的存贮方法错误的是( )
| A、金属钠保存在石蜡油或煤油中 |
| B、用铁制或铝制容器运输浓硫酸、浓硝酸 |
| C、FeCl2溶液的试剂瓶中要放铁钉 |
| D、氢氧化钠溶液盛装在玻璃塞的试剂瓶中 |
考点:化学试剂的存放
专题:
分析:A.钠化学性质活泼,需要隔绝空气、水,采用密封保存;
B.常温下,Fe、Al遇浓硫酸发生钝化;
C.铁离子能和铁反应生成亚铁离子;
D.氢氧化钠能够与玻璃中的二氧化硅发生反应.
B.常温下,Fe、Al遇浓硫酸发生钝化;
C.铁离子能和铁反应生成亚铁离子;
D.氢氧化钠能够与玻璃中的二氧化硅发生反应.
解答:
解:A.钠需要隔绝空气密封保存,钠的密度大于煤油和石蜡,可以保存在煤油或者石蜡中,故A正确;
B.常温下,Fe、Al遇浓硫酸、浓硝酸发生钝化,生成致密的氧化膜阻止反应的进一步发生,则用铁制或铝制容器运输浓硫酸、浓硝酸,故B正确;
C.铁离子能和铁反应生成亚铁离子,可防止亚铁离子被氧化,故C正确;
D.氢氧化钠能够与二氧化硅反应生成硅酸钠,硅酸钠能够将玻璃瓶与玻璃塞粘在一起,所以盛放氢氧化钠溶液不能使用玻璃塞,应该使用橡胶塞,故D错误.
故选D.
B.常温下,Fe、Al遇浓硫酸、浓硝酸发生钝化,生成致密的氧化膜阻止反应的进一步发生,则用铁制或铝制容器运输浓硫酸、浓硝酸,故B正确;
C.铁离子能和铁反应生成亚铁离子,可防止亚铁离子被氧化,故C正确;
D.氢氧化钠能够与二氧化硅反应生成硅酸钠,硅酸钠能够将玻璃瓶与玻璃塞粘在一起,所以盛放氢氧化钠溶液不能使用玻璃塞,应该使用橡胶塞,故D错误.
故选D.
点评:本题考查了常见化学试剂的保存方法,题目难度不大,注意掌握常见化学试剂的化学性质及正确保存方法,如碱性溶液需要使用橡胶塞,氢氟酸不能使用玻璃瓶等.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
下列有机反应中,有一项反应类型不同于其他三项的是( )
A、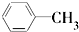 +Cl2 +Cl2
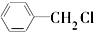 +HCl +HCl | |||
B、2CH3CH2OH+O2
| |||
C、ClCH2CH=CH2+NaOH
| |||
D、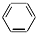 +HONO2 +HONO2
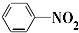 +H2O +H2O |
下列关于Na2O和Na2O2 的说法中,正确的是( )
| A、均能与水反应 |
| B、氧元素的化合价均为-2 |
| C、均为淡黄色固体 |
| D、均能与CO2反应放出氧气 |
一定量的混合气体,在密闭容器中发生如下反应:xA(g)+yB(g)?zC(g),达到平衡后测得A气体的浓度为2.5mol/L,当恒温下将密闭容器的容积缩小到原体积
时,再达到平衡后,测得A浓度为4.5mol/L,则下列叙述正确的是( )
| 1 |
| 2 |
| A、平衡向逆反应方向移动 |
| B、x+y<z |
| C、C的体积分数提高 |
| D、B的转化率降低 |
下列操作中,能使电离平衡:H2O═H++OH-,向右移动且溶液呈酸性的是( )
| A、向水中加入Na2CO3溶液 |
| B、向水中加入Al2(SO4)3固体 |
| C、向水中加入NaHSO4溶液 |
| D、将水加热到100℃,使pH=6 |
1molH2在O2中燃烧生成液态水放出285.8kJ的热量,则下列热化学方程式正确的是( )
| A、2H2(g)+O2(g)=2H2O(l)△H=+571.6kJ?mol-1 | ||
| B、2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ?mol-1 | ||
C、H2(g)+
| ||
D、H2(g)+
|
设NA表示阿伏加德罗常数的值,下列有关说法正确的是( )
| A、同温同压下,原子数均为NA的氢气和氦气具有相同的体积 |
B、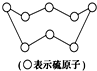 32gS8单质中含有的S-S键个数为NA(见图) |
| C、10L 0.1mol/L Na2S的水溶液中,S2-、HS-两种微粒数之和为NA个 |
| D、标准状况下,22.4LNO和11.2LO2混合后气体的分子总数为1.5NA |
