题目内容
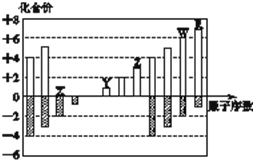 如图所示是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
如图所示是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )| A、原子半径:Z>Y>X |
| B、气态氢化物的稳定性:R>W |
| C、WX3和水反应形成的化合物是离子化合物 |
| D、Y和Z两者最高价氧化物对应的水化物不能相互反应 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由表中化合价可知,X的化合价为-2价,没有正化合价,故X为O元素,Y的化合价为+1价,处于ⅠA族,原子序数大于O元素,故Y为Na元素,Z为+3价,为Al元素,W的化合价为+6、-2价,故W为S元素,R的最高正价为+7价,应为Cl元素,结合对应单质、化合物的性质以及题目要求解答该题.
解答:
解:由表中化合价可知,X的化合价为-2价,没有正化合价,故X为O元素,Y的化合价为+1价,处于ⅠA族,原子序数大于O元素,故Y为Na元素,Z为+3价,为Al元素,W的化合价为+6、-2价,故W为S元素,R的最高正价为+7价,应为Cl元素,所以X为O,Y为Na,Z为Al,W为S,R为Cl;
A.已知X为O,Y为Na,Z为Al,所以原子半径应为Na>Al>O,故A错误;
B.已知W为S,R为Cl,所以非金属性Cl>S,则气态氢化物的稳定性Cl>S,故B正确;
C.X为O,W为S,所以WX3和水反应形成的化合物是硫酸,是共价化合物,故C错误;
D.Z为Al,Y为Na,两者最高价氧化物对应的水化物是NaOH和Al(OH)3,二者能反应生成偏铝酸钠和水,故D错误;
故选:B.
A.已知X为O,Y为Na,Z为Al,所以原子半径应为Na>Al>O,故A错误;
B.已知W为S,R为Cl,所以非金属性Cl>S,则气态氢化物的稳定性Cl>S,故B正确;
C.X为O,W为S,所以WX3和水反应形成的化合物是硫酸,是共价化合物,故C错误;
D.Z为Al,Y为Na,两者最高价氧化物对应的水化物是NaOH和Al(OH)3,二者能反应生成偏铝酸钠和水,故D错误;
故选:B.
点评:本题考查结构性质与位置关系、元素周期律等,难度不大,根据化合价推断元素是解题的关键.

练习册系列答案
相关题目
向某无色溶液中分别进行下列操作,所得现象和结论正确的是( )
| A、加入氨水,产生白色沉淀,证明原溶液中存在Al3+ |
| B、加入AgNO3溶液,产生白色沉淀,证明原溶液中存在Cl- |
| C、加入盐酸酸化的BaCl2溶液,生成白色沉淀,证明原溶液中存在SO42- |
| D、加入NaOH溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,证明原溶液中存在NH4+ |
在一定条件下,反应N2+3H2═2NH3在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为( )
| A、v(H2)=0.03mol?L-1?min-1 |
| B、v(N2)=0.02mol?L-1?min-1 |
| C、v(NH3)=0.17mol?L-1?min-1 |
| D、v(NH3)=0.01mol?L-1?min-1 |
下列物质不属于大气污染物的是( )
| A、二氧化硫 | B、二氧化碳 |
| C、二氧化氮 | D、一氧化碳 |
硒(Se)是硫的同族元素,有关SeO2的两个化学反应如下.下列有关叙述正确的是( )
①SeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2O
②Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O.
①SeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2O
②Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O.
| A、①中Se是氧化产物,I2是还原产物 |
| B、SeO2、H2SO4(浓)、I2的氧化性由强到弱的顺序是I2>SeO2>H2SO4(浓) |
| C、常温常压下,Se是固体,其最高价氧化物对应的水化物是H2SeO4 |
| D、反应①中每有0.6mol I2生成,转移电子数目为2.4NA |
在碳酸钠的饱和溶液中,C(Na+)和C(CO32-)的比值( )
| A、等于1 | B、等于2 |
| C、大于2 | D、1-2之间 |
