题目内容
下列各实验装置图与操作正确且能达到实验目的是( )

| A、待KNO3热饱和溶液冷却 |
| B、用工业酒精制取无水乙醇结晶后进行快速过滤 |
| C、实验室收集SO2气体 |
| D、实验室干燥氨气 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.安全瓶应长进短出;
B.温度计位置错误;
C.SO2气体密度比空气大;
D.氢氧化钠与氨气不反应.
B.温度计位置错误;
C.SO2气体密度比空气大;
D.氢氧化钠与氨气不反应.
解答:
解:A.安全瓶应长进短出,右端用短导管,故A错误;
B.蒸馏时,温度计用于测量馏分的温度,温度计水银球应位于蒸馏烧瓶的支管口附近,故B错误;
C.SO2气体密度比空气大,应用向上排空气法收集,故C错误;
D.氧化钠与氨气不反应,可干燥氨气,故D正确.
故选D.
B.蒸馏时,温度计用于测量馏分的温度,温度计水银球应位于蒸馏烧瓶的支管口附近,故B错误;
C.SO2气体密度比空气大,应用向上排空气法收集,故C错误;
D.氧化钠与氨气不反应,可干燥氨气,故D正确.
故选D.
点评:本题考查较为综合,涉及气体的除杂、分离,物质的制备等,综合考查学生的分析能力、实验能力和评价能力,为高考常见题型,注意把握物质的性质的异同以及实验的严密性和可行性的评价,难度不大.

练习册系列答案
相关题目
可逆反应 H2 (g)+I2 (g)?2HI(g),温度一定,在1L的密闭容器中加入2molH2(g)和1molI2(g)开始反应,2min末测知容器中生成了1.2mol HI(g),下列说法正确的是( )
| A、H2(g)的消耗速率与I2(g)的生成速率始终相等 |
| B、反应过程中,H2(g)和I2(g)的转化率始终相等 |
| C、平衡前,正、逆反应速率的比值恒定 |
| D、反应开始至2min末,v(H2)=0.3mol?L-1?min-1 |
下列说法不正确的是( )
| A、可逆反应在一定条件下有一定的限度,当反应进行到一定限度后,反应物不再转化为生成物 |
| B、决定化学反应速率的主要因素是参加反应的物质的性质 |
| C、化学反应的速率和限度均可通过改变化学反应条件而改变 |
| D、化学反应达到平衡状态时,只要条件不改变,各物质的浓度就不再改变 |
仅改变下列一个条件,通过提高活化分子的百分率来提高反应速率的是( )
| A、降温 | B、加压 |
| C、加催化剂 | D、加大反应物浓度 |
有机物A和B是正处于临床试验阶段的小分子抗癌药物,结构如图所示,关于有机物A和B的叙述,正确的是( )
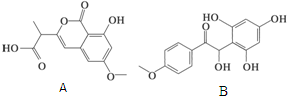

| A、二者都能与Br2发生反应,等物质的量A和B最多消耗的Br2的比例为2:3 |
| B、有机物A和B既可以与FeCl3溶液发生显色反应,又可以和NaHCO3溶液反应 |
| C、1 mol B最多能与6 mol氢气反应 |
| D、等物质的量A和B最多消耗的氢氧化钠质量比为1:1 |