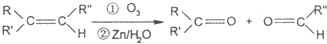
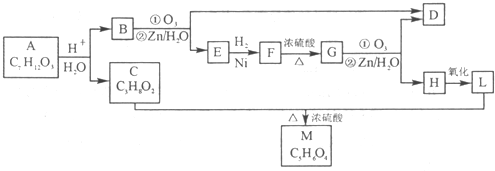
题目内容
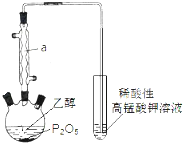 已知用P2O5作催化剂,加热乙醇可制备乙烯,反应温度为80℃~210℃.某研究性小组设计了如下的装置制备并检验产生的乙烯气体(夹持和加热仪器略去).
已知用P2O5作催化剂,加热乙醇可制备乙烯,反应温度为80℃~210℃.某研究性小组设计了如下的装置制备并检验产生的乙烯气体(夹持和加热仪器略去).(1)仪器a的名称为
(2)用化学反应方程式表示上述制备乙烯的原理
(3)已知P2O5是一种酸性干燥剂,吸水放出大量热,在实验过程中P2O5与乙醇能发生作用,因反应用量的不同,会生成不同的磷酸酯,它们均为易溶于水的物质,沸点较低.写出乙醇和磷酸反应生成磷酸二乙酯的化学方程式(磷酸用结构式表示
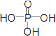 )
)(4)该装置中还缺一种必备仪器,该仪器为
考点:乙醇的消去反应
专题:实验题
分析:(1)乙醇易挥发,需要冷凝装置,根据仪器A的构造写出其名称;
(2)乙醇在P2O5作催化剂的催化作用下发生分子内脱水制取乙烯,反应原理与浓硫酸作催化剂相似;
(3)根据酯化反应规律为醇羟基去氢和酸酸去羟基,剩余部分连在一起,写出反应方程式;
(4)该反应中需要控制温度80℃~210℃,必须使用温度计;
制得的乙烯气体中通常会含有乙醇、CO2、SO2等气体,乙醇、二氧化硫和高锰酸钾都能发生氧化还原反应,导致高锰酸钾褪色,干扰了乙烯的检验.
(2)乙醇在P2O5作催化剂的催化作用下发生分子内脱水制取乙烯,反应原理与浓硫酸作催化剂相似;
(3)根据酯化反应规律为醇羟基去氢和酸酸去羟基,剩余部分连在一起,写出反应方程式;
(4)该反应中需要控制温度80℃~210℃,必须使用温度计;
制得的乙烯气体中通常会含有乙醇、CO2、SO2等气体,乙醇、二氧化硫和高锰酸钾都能发生氧化还原反应,导致高锰酸钾褪色,干扰了乙烯的检验.
解答:
解:(1)乙醇易挥发,故需要冷凝管,A为球形冷凝管(或冷凝管),故答案为:球形冷凝管(或冷凝管);
(2)利用乙醇在P2O5作催化剂的催化作用下发生分子内脱水制取乙烯,反应原理与浓硫酸作催化剂相似,只是反应条件不同,
乙醇发生了消去反应,反应方程式为: ,
,
故答案为: ;
;
(3)根据酯化反应规律为醇羟基去氢和酸去羟基,剩余部分连在一起,写出乙醇和磷酸反应生成磷酸二乙酯的化学方程式为: ,
,
故答案为: ;
;
(4)根据“加热乙醇可制备乙烯,反应温度为80℃~210℃”可知,需要测定控制反应温度,则必须使用温度计,所以该装置中还缺少的仪器为温度计;
乙醇具有挥发性,乙烯中可能混有乙醇,浓硫酸具有强氧化性,能氧化乙醇,把乙醇氧化成碳,同时自身被还原成二氧化硫,
乙醇、二氧化硫和乙烯都能被高锰酸钾溶液氧化,导致高锰酸钾溶液褪色,所以此装置不够严密,应先除去乙烯中混有乙醇和二氧化硫再检验乙烯,
故答案为:温度计;没有排除乙醇的干扰(或没有排除二氧化硫的干扰).
(2)利用乙醇在P2O5作催化剂的催化作用下发生分子内脱水制取乙烯,反应原理与浓硫酸作催化剂相似,只是反应条件不同,
乙醇发生了消去反应,反应方程式为:
 ,
,故答案为:
 ;
;(3)根据酯化反应规律为醇羟基去氢和酸去羟基,剩余部分连在一起,写出乙醇和磷酸反应生成磷酸二乙酯的化学方程式为:
 ,
,故答案为:
 ;
;(4)根据“加热乙醇可制备乙烯,反应温度为80℃~210℃”可知,需要测定控制反应温度,则必须使用温度计,所以该装置中还缺少的仪器为温度计;
乙醇具有挥发性,乙烯中可能混有乙醇,浓硫酸具有强氧化性,能氧化乙醇,把乙醇氧化成碳,同时自身被还原成二氧化硫,
乙醇、二氧化硫和乙烯都能被高锰酸钾溶液氧化,导致高锰酸钾溶液褪色,所以此装置不够严密,应先除去乙烯中混有乙醇和二氧化硫再检验乙烯,
故答案为:温度计;没有排除乙醇的干扰(或没有排除二氧化硫的干扰).
点评:本题考查了乙醇的消去反应的实验,属于拓展教材内容的典型实验,题目难度不大,明确题中所给的信息为解答本题的关键,试题测重学生基本实验操作能力的考查,培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、常温常压下,0.1NA个HCl分子的体积为2.24L |
| B、标准状况下,22.4L 氖气含有2NA 个原子 |
| C、1L 0.2mol/L 硫酸铁溶液中含有的SO42- 离子数目为0.2 NA |
| D、1 mol氖中含有的电子数为10NA |
下列叙述正确的是( )
| A、可以根据PbI2和AgCl的Ksp的大小比较两者的溶解度 |
| B、常温下,同浓度的Na2S与NaHS溶液相比,NaHS溶液的pH大 |
| C、等物质的量浓度的CH3COONH4溶液和NH4HSO4溶液,前者的c(NH4+)小 |
| D、用惰性电极电解饱和NaCl溶液,若有1.0 mol电子转移,则理论生成1.0 mol NaOH |
对已达平衡的反应2X(g)+Y(g)?4Z(g),改变以下哪种条件能使速率变化如图所示( )


| A、增大Z的浓度 |
| B、减小X的浓度 |
| C、增大压强 |
| D、减小压强 |
已知298K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,现取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀平衡时,测得溶液的pH=13,则下列说法不正确的是( )
| A、所得溶液中由水离出的C(OH-)=1.0×10-13mol?L-1 |
| B、所加烧碱溶液的pH=13 |
| C、所得溶液中C(Mg2+)=5.6×10-10mol?L-1 |
| D、在整个反应过程中,H2O的电离度在逐渐减小 |
为达到预期的实验目的,下列操作正确的是( )
| A、欲配制质量分数为10%的ZnSO4溶液,将5g ZnSO4溶解在45g水中 |
| B、在25℃温度条件下,配制100g溶解度为25g的NaCl饱和溶液,将25g的NaCl溶解在75g水中 |
| C、加热蒸发质量分数为10%的盐酸,可得到质量分数为36.5%的浓盐酸 |
| D、向25℃的饱和CuSO4溶液中加入CuSO4粉末,制备CuSO4?5H2O晶体 |
室温下,某溶液中由水电离产生c(H+)=10-13 mol.L-1,该溶液的溶质不可能是( )
| A、NaHSO4 |
| B、NaCl |
| C、HCl |
| D、Ba(OH)2 |
 在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中含有大量Mg2+、Al3+、Fe3+、Ag+、Ba2+等离子.试分析回答下列问题:
在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中含有大量Mg2+、Al3+、Fe3+、Ag+、Ba2+等离子.试分析回答下列问题: