题目内容
3.某烃中含有碳原子数为3,且含碳元素的质量分数为85.7%,且在空气燃烧时有大量黑烟(M空气设为29).(1)该烃的分子式为C3H6,若该烃能使高锰酸钾溶液褪色,其结构简式可能为CH3CH=CH2.
(2)该烯烃与溴单质加成的方程式为CH3CH=CH2+Br2→CH3CHBrCH2Br.
分析 烃中含有碳原子数为3,且含碳元素的质量分数为85.7%,则相对分子质量为$\frac{3×12}{85.7%}$=42,则H原子个数为$\frac{42-36}{1}$=6,应为C3H6,结构简式为CH3CH=CH2,含有碳碳双键,可发生氧化反应和加成反应,以此解答该题.
解答 解:(1)烃中含有碳原子数为3,且含碳元素的质量分数为85.7%,则相对分子质量为$\frac{3×12}{85.7%}$=42,则H原子个数为$\frac{42-36}{1}$=6,应为C3H6,结构简式为CH3CH=CH2,故答案为:C3H6;CH3CH=CH2;
(2)CH3CH=CH2含有碳碳双键,可与溴发生加成反应,方程式为CH3CH=CH2+Br2→CH3CHBrCH2Br,故答案为:CH3CH=CH2+Br2→CH3CHBrCH2Br.
点评 本题考查有机物的推断,侧重于结构和性质的考查,有利于培养学生的分析能力和计算能力,注意把握有机物官能团的性质,难度不大.

练习册系列答案
相关题目
14.NA表示阿伏伽德罗常数,某氯气样品由37Cl2分子组成,下列说法正确的是( )
| A. | 37g该氯气样品含NA个氯气分子 | |
| B. | 11.2L该氯气样品质量是37g | |
| C. | 37g该氯气样品与足量NaOH完全反应生成Na37Cl和Na37ClO3,氧化剂和还原剂的质量之比为5:1 | |
| D. | 0.1NA个氯气分子溶于水形成1000mL溶液,溶液中c(Cl-)=0.2mol/L |
11.下列化学用语正确的是( )
| A. | 乙烯的结构简式:C2H4 | B. | NaH中氢离子的结构示意图: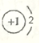 | ||
| C. | NH4I的电子式: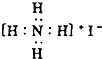 | D. | H2O、CO2的比例模型都可以用 表示 表示 |
18.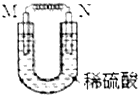 如图所示装置中,M为活动性顺序位于氢之前的金属,N为石墨棒.关于此装置的下列叙述中,不正确的是( )
如图所示装置中,M为活动性顺序位于氢之前的金属,N为石墨棒.关于此装置的下列叙述中,不正确的是( )
 如图所示装置中,M为活动性顺序位于氢之前的金属,N为石墨棒.关于此装置的下列叙述中,不正确的是( )
如图所示装置中,M为活动性顺序位于氢之前的金属,N为石墨棒.关于此装置的下列叙述中,不正确的是( )| A. | N上有气体放出 | |
| B. | M为负极,N为正极 | |
| C. | 导线中有电流通过,电流方向是由M到N | |
| D. | 该装置是化学能转变为电能的装置 |
8.实验室中,下列药品保存方法正确的是( )
①白磷保存在冷水中
②钠,钾保存在水里
③HF溶液保存在塑料瓶中
④Na2CO3溶液保存在带橡胶塞的试剂瓶内
⑤浓硝酸保存在棕色广口瓶内.
①白磷保存在冷水中
②钠,钾保存在水里
③HF溶液保存在塑料瓶中
④Na2CO3溶液保存在带橡胶塞的试剂瓶内
⑤浓硝酸保存在棕色广口瓶内.
| A. | ①③④ | B. | ③④ | C. | ①②③④ | D. | ①②③④⑤ |
5.某原电池总反应的离子方程式为Cu2++Fe=Fe2++Cu能实现该反应的原电池组成是( )
| A. | 正极为铁,负极为铁,电解质溶液为CuCl2溶液 | |
| B. | 正极为银,负极为铁,电解质液为Fe(NO3)3溶液 | |
| C. | 正极为碳,负极为锌,电解质溶液为Fe2(SO4)3溶液 | |
| D. | 正极为碳,负极为铁,电解质溶液为CuSO4溶液 |

 图是超导化合物----钙钛矿晶体中最小重复单元(晶胞)的结构.该化合物的化学式为CaTiO3.在该晶体中,与某个钛离子距离最近且相等的其他钛离子共有6个.
图是超导化合物----钙钛矿晶体中最小重复单元(晶胞)的结构.该化合物的化学式为CaTiO3.在该晶体中,与某个钛离子距离最近且相等的其他钛离子共有6个.