题目内容
11.X、Y是元素周期表第VIIA族的两种元素,下列说法中能说明X的非金属性比Y强的是( )| A. | X元素原子的电子层数比Y元素原子的电子层数多 | |
| B. | X的气态氢化物比Y的气态氢化物稳定 | |
| C. | X的最高价氧化物对应水化物的酸性比Y的弱 | |
| D. | Y的单质能将X从NaX溶液中置换出来 |
分析 元素的非金属性越强,其最高价氧化物的水化物酸性越强、其单质的氧化性越强、其单质与氢气化合越容易、其氢化物的稳定性越强,据此分析解答.
解答 解:A.X元素原子的电子层数比Y元素原子的电子层数多,但非金属性X不一定比Y强,如Si和O元素,故A错误;
B.元素的非金属性越强其氢化物越稳定,X的气态氢化物比Y的气态氢化物稳定,说明非金属性X>Y,故B正确;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,X的最高价氧化物对应水化物的酸性比Y的弱,说明非金属性X<Y,故C错误;
D.Y的单质能将X从NaX溶液中置换出来,说明Y单质的氧化性大于X,所以非金属性X<Y,故D错误;
故选B.
点评 本题考查元素周期律,为高频考点,明确非金属性强弱与得电子难易程度有关,与得电子多少无关,易错选项是A.

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案
相关题目
2.下列说法正确的是( )
①离子化合物含离子键,也可能含极性键或非极性键
②共价化合物含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥离子化合物在熔融状态能导电.
①离子化合物含离子键,也可能含极性键或非极性键
②共价化合物含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥离子化合物在熔融状态能导电.
| A. | ①③⑥ | B. | ②④⑥ | C. | ②③④ | D. | ①③⑤ |
19.下列物质中属于共价化合物的是( )
| A. | NaCl | B. | KOH | C. | Cl2 | D. | CO2 |
6.下列有关三氧化硫的说法中,正确的是( )
| A. | 三氧化硫极易溶于水,且与水反应生成H2SO3 | |
| B. | SO3属于酸性氧化物 | |
| C. | 硫粉在过量的氧气中燃烧生成SO3 | |
| D. | SO2、SO3均具有漂白性,能使紫色石蕊溶液褪色 |
16.下列有关粒子的表示方法正确的是( )
| A. | 氨气分子的电子式: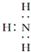 | B. | 硫原子结构示意图: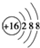 | ||
| C. | 次氯酸的结构式:H-O-Cl | D. | H2O的电子式: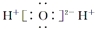 |
3.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g);△H=+49.0kJ•mol-1
②CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g);△H=-192.9kJ•mol-1
下列说法正确的是( )
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g);△H=+49.0kJ•mol-1
②CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g);△H=-192.9kJ•mol-1
下列说法正确的是( )
| A. | CH3OH的燃烧热为192.9kJ•mol-1 | |
| B. | CH3OH转变成H2的过程一定要吸收能量 | |
| C. | 可推知2H2(g)+O2(g)═2H2O(g)△H=-483.8 kJ/mol | |
| D. | 根据②推知反应:CH3OH(l)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)的△H<-192.9kJ•mol-1 |
20.“达菲”是瑞士罗氏公司研制的有效治疗人类禽流感的药物.达菲的主要合成原料是我国盛产的莽草酸.
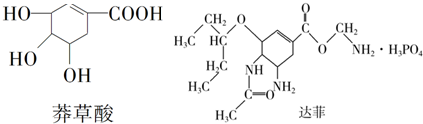
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 莽草酸可溶于水 | |
| B. | 1 mol莽草酸最多可和4 molNaOH溶液反应 | |
| C. | 从结构上推测,达菲既可与盐酸反应又可与氢氧化钠溶液反应 | |
| D. | 从结构上推测,以莽草酸为原料合成达菲须经过酯化反应等步骤 |
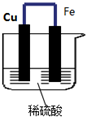 如图所示,将铁、铜通过导线相连,置于稀硫酸中.
如图所示,将铁、铜通过导线相连,置于稀硫酸中.