题目内容
(1)将1.02g Mg、Al的混合物投入盛有过量NaOH溶液的烧杯中,充分反应后得到672mL 氢气(标准状况下),此时发生反应的离子方程式是 ;
(2)将上述烧杯中的浊液过滤,向滤液中逐滴加入盐酸过量,产生的现象是 ,发生反应的离子方程式是 .
(2)将上述烧杯中的浊液过滤,向滤液中逐滴加入盐酸过量,产生的现象是
考点:铝的化学性质,离子方程式的书写
专题:几种重要的金属及其化合物
分析:(1)Mg和NaOH不反应,Al和NaOH溶液反应生成偏铝酸钠和氢气;
(2)滤液中溶质成分是偏铝酸钠、NaOH,向混合溶液中滴加稀盐酸至过量,稀盐酸先和NaOH反应生成氯化钠,然后再和偏铝酸钠生成氢氧化铝沉淀,最后稀盐酸和氢氧化铝沉淀反应生成氯化铝.
(2)滤液中溶质成分是偏铝酸钠、NaOH,向混合溶液中滴加稀盐酸至过量,稀盐酸先和NaOH反应生成氯化钠,然后再和偏铝酸钠生成氢氧化铝沉淀,最后稀盐酸和氢氧化铝沉淀反应生成氯化铝.
解答:
解:(1)Mg和NaOH不反应,Al和NaOH溶液反应生成偏铝酸钠和氢气,离子方程式为2Al+2OH-+2H2O=2NaAlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2NaAlO2-+3H2↑;
(2)滤液中溶质成分是偏铝酸钠、NaOH,向混合溶液中滴加稀盐酸至过量,稀盐酸先和NaOH反应生成氯化钠,然后再和偏铝酸钠生成氢氧化铝沉淀,最后稀盐酸和氢氧化铝沉淀反应生成氯化铝,所以看到的现象是先没有沉淀生成、反应一段时间后有白色沉淀生成、最终白色沉淀溶解,涉及的离子方程式为OH-+H+=H2O、AlO2-+H++H2O=Al(OH)3↓、Al(OH)3+3H+=Al3++3H2O,
故答案为:先没有沉淀生成、反应一段时间后有白色沉淀生成、最终白色沉淀溶解;OH-+H+=H2O、AlO2-+H++H2O=Al(OH)3↓、Al(OH)3+3H+=Al3++3H2O.
(2)滤液中溶质成分是偏铝酸钠、NaOH,向混合溶液中滴加稀盐酸至过量,稀盐酸先和NaOH反应生成氯化钠,然后再和偏铝酸钠生成氢氧化铝沉淀,最后稀盐酸和氢氧化铝沉淀反应生成氯化铝,所以看到的现象是先没有沉淀生成、反应一段时间后有白色沉淀生成、最终白色沉淀溶解,涉及的离子方程式为OH-+H+=H2O、AlO2-+H++H2O=Al(OH)3↓、Al(OH)3+3H+=Al3++3H2O,
故答案为:先没有沉淀生成、反应一段时间后有白色沉淀生成、最终白色沉淀溶解;OH-+H+=H2O、AlO2-+H++H2O=Al(OH)3↓、Al(OH)3+3H+=Al3++3H2O.
点评:本题以铝为载体考查离子方程式的书写,明确物质的性质是解本题关键,注意(2)中离子反应先后顺序,知道氢氧化铝的两性,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
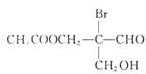 有机物若含手性碳原子(连接四个不同的原子或原子团的碳原子)就具有光学活性,如图物质发生下列反应后生成的有机物仍有光学活性的是( )
有机物若含手性碳原子(连接四个不同的原子或原子团的碳原子)就具有光学活性,如图物质发生下列反应后生成的有机物仍有光学活性的是( )①与甲酸、浓硫酸共热 ②与NaOH水溶液共热 ③与银氨溶液作用
④在Cu催化下与O2共热 ⑤在Ni催化下与氢气反应.
| A、仅③ | B、仅①③ |
| C、仅②④⑤ | D、①②③④⑤ |
下列叙述中,正确的是( )
| A、在AgBr饱和溶液中加入AgNO3溶液,达到平衡时,溶液中Br-浓度降低 |
| B、常温下,某溶液中由水电离出的c(OH-)=1×10-10mol/L,该溶液一定呈酸性 |
| C、FeCl3溶液和Fe2(SO4)3溶液加热蒸干,灼烧都得到Fe2O3 |
| D、向饱和碳酸钠溶液中通入足量二氧化碳,可以析出纯碱晶体 |
下列命名正确的是( )
| A、2,4,4-三甲基戊烷 |
| B、4-甲基-2-乙基辛烷 |
| C、2-甲基-1,3-丁二烯 |
| D、2-甲基-1-丙烯 |
在下列物质中,分别加入金属钠,不能产生氢气的是( )
| A、蒸馏水 | B、乙酸 |
| C、无水乙醇 | D、苯 |
工业上利用N2和H2反应制取NH3,下列措施不能加快该反应的反应速率的是( )
| A、升高温度 |
| B、增大压强 |
| C、将NH3及时分离 |
| D、使用催化剂 |
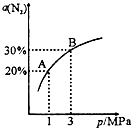 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α%)与体系总压强(P)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α%)与体系总压强(P)的关系如图所示.下列说法正确的是( )| A、将1.0mol氮气和3.0mol氢气,置于1L密闭容器中发生反应,放出的热量为92.4kJ |
| B、平衡状态由A变到B时,平衡常数K(A)<K(B) |
| C、上述反应在达到平衡后,增大压强,H2的转化率提高 |
| D、升高温度,平衡向逆反应方向移动 |