题目内容
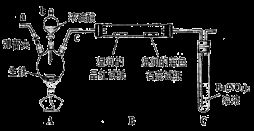
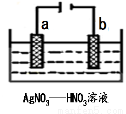
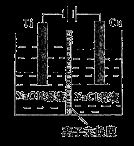
纳米级Cu2O由于具有优良的催化性能而受到关注。采用离子交换膜控制电解液中OH一的浓度制备纳米级Cu2O的装置如图所示,发生的反应为:2Cu+H2O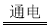 Cu2O+H2↑。下列说法正确的是
Cu2O+H2↑。下列说法正确的是
A.钛电极发生氧化反应
B.阳极附近溶液的pH逐渐增大
C.离子交换膜应采用阳离子离子交换膜
D.阳极反应式是:2Cu+2OH一一2e一== Cu2O+H2O
D
【解析】
试题分析:A根据题图可知:Ti与电源的负极连接,是阴极,在阴极上发生还原反应,错误;B.Cu电极与电源的正极连接,作阳极,由于Cu是活性电极,所以在阳极发生反应:Cu-2e-=Cu2+,然后与溶液中的OH-发生反应:2Cu2++2OH-= Cu2O+H2O,该电极的总方程式是:2Cu+2OH一一2e一== Cu2O+H2O,由于溶液中的OH-离子不断消耗,所以附近的溶液的pH减小,错误;C.若离子交换膜采用阳离子离子交换膜,OH-就不能与阳极产生的Cu2+发生反应产生Cu2O,所以应该采用阴离子交换膜,错误,D.根据B选项分析可知阳极电极反应式是:2Cu+2OH一一2e一== Cu2O+H2O,正确。
考点:考查电解法制取纳米级Cu2O的反应原理的知识。

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
 原子半径最大,元素D的
原子半径最大,元素D的 合金是日常生活中常用的金属材料。下列说法正确的是
合金是日常生活中常用的金属材料。下列说法正确的是