题目内容
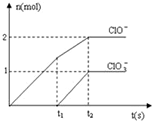 在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、ClO-、ClO
在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、ClO-、ClO- 3 |
- 3 |
| A、0~t1时,Ca(OH)2与Cl2发生反应的总化学方程式为2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O | ||
B、t2时,Cl-与ClO
| ||
| C、该石灰乳中含有Ca(OH)2的物质的量为10mol | ||
| D、由图可知,生成Ca(ClO3)2的反应是由温度升高引起的 |
考点:氧化还原反应的计算,氯、溴、碘及其化合物的综合应用
专题:图示题
分析:A.0~t1时,不生成ClO3-;
B.由图可知,t2时n(ClO-)=2mol,n(ClO3-)=1mol,失去电子为2mol×1+1mol×5=7mol,则Cl-得到电子为7mol;
C.由B可知,n(ClO-)=2mol,n(ClO3-)=1mol,n(Cl-)=7mol,由n(Ca(OH)2)=n(Cl2)计算;
D.开始生成次氯酸根离子,该反应为放热反应,温度升高,t2时开始生成氯酸根离子.
B.由图可知,t2时n(ClO-)=2mol,n(ClO3-)=1mol,失去电子为2mol×1+1mol×5=7mol,则Cl-得到电子为7mol;
C.由B可知,n(ClO-)=2mol,n(ClO3-)=1mol,n(Cl-)=7mol,由n(Ca(OH)2)=n(Cl2)计算;
D.开始生成次氯酸根离子,该反应为放热反应,温度升高,t2时开始生成氯酸根离子.
解答:
解:A.0~t1时,不生成ClO3-,则Ca(OH)2与Cl2发生反应的总化学方程式为2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O,故A正确;
B.由图可知,t2时n(ClO-)=2mol,n(ClO3-)=1mol,失去电子为2mol×1+1mol×5=7mol,则Cl-得到电子为7mol,t2时,Cl-与ClO3-的个数比为7:1,故B正确;
C.由B可知,n(ClO-)=2mol,n(ClO3-)=1mol,n(Cl-)=7mol,由n(Ca(OH)2)=n(Cl2)可知,n(Ca(OH)2)=
×(1+7+2)=5mol,故C错误;
D.开始生成次氯酸根离子,该反应为放热反应,温度升高,t2时开始生成氯酸根离子,则生成Ca(ClO3)2的反应是由温度升高引起的,故D正确;
故选C.
B.由图可知,t2时n(ClO-)=2mol,n(ClO3-)=1mol,失去电子为2mol×1+1mol×5=7mol,则Cl-得到电子为7mol,t2时,Cl-与ClO3-的个数比为7:1,故B正确;
C.由B可知,n(ClO-)=2mol,n(ClO3-)=1mol,n(Cl-)=7mol,由n(Ca(OH)2)=n(Cl2)可知,n(Ca(OH)2)=
| 1 |
| 2 |
D.开始生成次氯酸根离子,该反应为放热反应,温度升高,t2时开始生成氯酸根离子,则生成Ca(ClO3)2的反应是由温度升高引起的,故D正确;
故选C.
点评:本题考查氧化还原反应的计算,为高频考点,把握图中离子的物质的量及对应的氧化还原反应为解答的关键,侧重分析、计算能力的考查,注意选项B、C中守恒法的应用,题目难度中等.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案
相关题目
下列有关实验操作、实验数据或实验事故的处理中正确的是( )(填序号).
| A、使用分液漏斗前不用检查活塞处是否漏水 |
| B、分液操作时,下层液体从下端放出,上层液体从上口倒出 |
| C、选用CCl4或酒精作为萃取剂从碘水中萃取碘 |
| D、为加速固体物质的溶解可采用粉碎、振荡、搅拌等方法 |
| E、蒸发NaCl溶液时,用玻棒搅拌防止液体局部过热引起飞溅 |
| F、配制H2SO4溶液时,先在量筒中加一定体积水,再慢慢加入浓H2SO4、及时搅拌 |
在10mL含等物质的量的HBr和H2SO3的溶液里通入0.01molCl2,有一半Br-变为Br2(已知Br2能氧化H2SO3).原溶液中HBr和H2SO3的浓度都等于( )mol?L-1.
| A、0.075 | B、0.8 |
| C、0.75 | D、0.08 |
质量分数2w,物质的量浓度为c1的H2SO4溶液加水稀释后,质量分数变为w,物质的量浓度变为c2,则c1( ) 2c2.
| A、大于 | B、小于 |
| C、等于 | D、无法确定 |
下面是四位同学对“化学与健康”这一话题发表的见解,正确的是( )
| A、多食用海产品可防治缺铁性贫血 |
| B、食物可调节人体细胞中的酸碱平衡 |
| C、为了减肥,我每天只吃水果、蔬菜 |
| D、我国应该禁止使用食物防腐剂 |
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )

| A、该硫酸的物质的量浓度为9.2mol/L |
| B、1molZn与足量的该硫酸反应产生2g氢气 |
| C、配制200mL4.6mol/L的稀硫酸需取该硫酸500mL |
| D、该硫酸与等质量的水混合所得溶液的物质的量浓度小于9.2mol/L |
下列各有机物的分类或命名正确的是( )
A、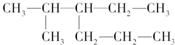 2甲基3丙基戊烷 2甲基3丙基戊烷 |
B、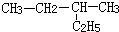 2-乙基丁烷 2-乙基丁烷 |
C、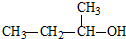 2-甲基-1-丙醇 2-甲基-1-丙醇 |
D、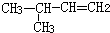 3-甲基-1-丁烯 3-甲基-1-丁烯 |
下列离子方程式中,正确的是( )
| A、将Na2O2固体投入H218O中:2H218O+2Na2O2=4OH-+4Na++18O2↑ |
| B、1mol/L的NaAlO2溶液和2.5 mol/L的HCl等体积互相均匀混合:2AlO2-+5 H+═Al(OH)3↓+Al3++H2O |
| C、碳酸氢钠溶液与少量氢氧化钡溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O |
| D、硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓ |