题目内容
3.下列材料的特性及用途说法错误的是(( )| A. | 高纯硅用于制造光导纤维,实现光电信号转化 | |
| B. | 石英中无色透明的晶体就是通常所说的水晶,其主要成分是二氧化硅 | |
| C. | 光导纤维导光的能力很强,是非常好的通讯材料 | |
| D. | 硅胶多孔,吸附水能力强,可以用作催化剂的载体 |
分析 A、光导纤维的材料为二氧化硅;
B、石英的主要成份是二氧化硅,二氧化硅是无色的晶体;
C、光导纤维传导光的能力非常强;
D、硅胶是硅酸凝胶经干燥脱水后得到的多孔固体,具有较强的吸附性.
解答 解:A、光导纤维的材料为二氧化硅,而晶体硅用于太阳能电池材料和集成电路材料,故A错误;
B、石英的主要成份是二氧化硅,二氧化硅是无色的晶体,故B正确;
C、光导纤维传导光的能力非常强,可传输光,故C正确;
D、硅胶是硅酸凝胶经干燥脱水后得到的多孔固体,具有较强的吸附性,可用于催化剂载体或干燥剂,故D正确;
故选A.
点评 本题考查无机非金属材料,题目难度不大,物质的成分决定物质的性质,注意基础知识的积累.

练习册系列答案
相关题目
13.为了测定铁铜合金的组成,将7.6g铁、铜合金加入100mL某浓度的稀硝酸中,将合金完全溶解后,共收集到NO气体2.24L(标准状况下),并测得溶液中H+的浓度为0.5mol•L-1,若反应前后溶液的体积变化忽略不计,则下列判断正确的是( )
| A. | 上述反应中金属共失去电子0.1mol | |
| B. | 合金中,铜的质量为2.8g | |
| C. | 原硝酸的浓度:c(HNO3)=4.5mol•L-1 | |
| D. | 要使溶液中的金属离子完全沉淀,需加5mol•L-1的NaOH溶液60mL |
14.“绿色化学”是指从技术、经济上设计可行的化学反应,尽可能减少对环境的负作用.下列化学反应中,不符合绿色化学概念的是( )
| A. | 消除制硝酸工业尾气中的氮氧化物的污染:NO+NO2+2NaOH═2NaNO2+H2O | |
| B. | 消除硫酸厂尾气中的SO2:SO2+2NH3•H2O═(NH4)2SO3+H2O | |
| C. | 用反应: 制备环氧乙烷 制备环氧乙烷 | |
| D. | 制CuSO4:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O |
11.如表对有关实验事实的解释或得出的结论合理的是( )
| 选项 | 实验事实 | 解释或结论 |
| A | KI淀粉溶液中滴入氯水变蓝,再通入SO2,溶液褪色 | SO2具有漂白性 |
| B | 将NaHCO3和NaAlO2溶液混合产生白色沉淀 | 酸性:HCO3->Al(OH)3 |
| C | 某钾盐溶于盐酸,产生无色无味气体,该气体通入 澄清石灰水,有白色沉淀出现 | 该钾盐是K2CO3 |
| D | NaI溶液$\stackrel{30%H_{2}O_{2}溶液}{→}$$\stackrel{稀硝酸及淀粉}{→}$溶液变蓝色 | 酸性条件下H2O2的氧化性比I2强 |
| A. | A | B. | B | C. | C | D. | D |
8. CuI是一种不溶于水的白色固体,它可以由反应2Cu2++4I-═2CuI↓+I2而得到.如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI淀粉溶液中阳极周围变蓝色,则下列说法正确的是( )
CuI是一种不溶于水的白色固体,它可以由反应2Cu2++4I-═2CuI↓+I2而得到.如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI淀粉溶液中阳极周围变蓝色,则下列说法正确的是( )
 CuI是一种不溶于水的白色固体,它可以由反应2Cu2++4I-═2CuI↓+I2而得到.如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI淀粉溶液中阳极周围变蓝色,则下列说法正确的是( )
CuI是一种不溶于水的白色固体,它可以由反应2Cu2++4I-═2CuI↓+I2而得到.如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI淀粉溶液中阳极周围变蓝色,则下列说法正确的是( )| A. | 若b极变红,则在Cu极上:Cu-2e-═Cu2+,Cu2+显蓝色 | |
| B. | 若a极变红,则在Pt电极上:2I--2e-═I2,淀粉遇碘变蓝 | |
| C. | 若a极变红,则在Cu电极上:开始Cu+I--e-═CuI,一段时间后2I--2e-═I2,淀粉遇碘变蓝 | |
| D. | 若b极变红,则在Pt电极上:4OH--4e-═2H2O+O2↑,O2将I-氧化为I2,淀粉遇碘变蓝 |
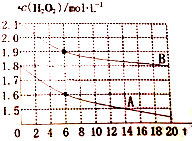 现有如下溶液:①1.0mL0.10mol•L-1双氧水 ②1.0mL0.20mol•L-1双氧水 ③3.0mL0.10mol•L-1KMnO4溶液 ④3.0mL0.010mol•L-1KMnO4溶液.所有实验均需加入1.0mL稀硫酸(足量),依据褪色时间长短判定反应速率快慢:
现有如下溶液:①1.0mL0.10mol•L-1双氧水 ②1.0mL0.20mol•L-1双氧水 ③3.0mL0.10mol•L-1KMnO4溶液 ④3.0mL0.010mol•L-1KMnO4溶液.所有实验均需加入1.0mL稀硫酸(足量),依据褪色时间长短判定反应速率快慢: .
.