题目内容
1.用 NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 常温常压下,48 g O2和 O3 含有的氧原子数均为 3NA | |
| B. | 将 0.1 mol 氯化铁溶于沸水中,所得溶液含 Fe(OH)3 胶粒数为 0.1 NA | |
| C. | 1.7 g 氨气所含有的电子数目为 10 NA | |
| D. | 22 g CO2与标准状况下 11.2 L H2O 含有相同分子数 |
分析 A.根据臭氧的质量计算出物质的量,再计算出含有的氧原子的物质的量及数目;
B.氯化铁溶液中铁离子部分水解,导致铁离子数目减少;
C.根据氨气的质量计算出氨气的物质的量及含有的电子数目;
D.标准状况下水不是气体.
解答 解:A.48g臭氧的物质的量为1mol,含有3mol氧原子,含有的氧原子数均为3NA,故A正确;
B.由于溶液中铁离子部分水解,将0.1mol氯化铁溶于1L水中,所得溶液含有铁离子物质的量小于0.1mol,铁离子数目小于0.1NA个,故B错误;
C.1.7g氨气的物质的量为0.1mol,含有1mol电子,所含有的电子数目为NA,故C错误;
D.22 g CO2物质的量=$\frac{22g}{44g/mol}$=0.5mol,标准状况下 11.2 L H2O 物质的量不是0.5mol,含有分子数不同,故D错误;
故选A.’
点评 本题考查了阿伏加德罗常数知识,题目难度不大,注意物质的组成、结构、状态、性质及存在条件等.

练习册系列答案
相关题目
9.化学与生活、环境等密切相关,下列有关说法错误的是( )
| A. | 用灼烧的方法可以区分蚕丝和人造纤维 | |
| B. | 食用油反复加热会产生稠环芳香烃等有害物质 | |
| C. | 近期在西非国家爆发的埃博拉疫情呈加速蔓延之势,已知该病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的 | |
| D. | 医用消毒酒精中乙醇的浓度为75% |
6.化学与环境、材料、信息、能源关系密切,下列说法中正确的是( )
| A. | 采煤作业上,把干冰和炸药放在一起,既能增强爆炸威力,又能防火灾 | |
| B. | 石油的分馏、煤的干馏等物理变化在生产中有着重要的地位 | |
| C. | 氢氧燃料电池、硅太阳能电池都利用了原电池原理 | |
| D. | 尽量使用12C的产品,减少使用含13C或14C的产品符合“促进低碳经济”宗旨 |
13.图中烧杯中盛的是天然水,铁腐蚀的速率由快到慢的顺序是( )


| A. | ⑤>②>①>③>④ | B. | ③>②>①>⑤>④ | C. | ⑤>②>③>④>① | D. | ③>④>⑤>②>① |
10.化学反应常伴有颜色变化,下列实验现象描述不正确的是( )
| A. | 将足量乙烯通入酸性高锰酸钾溶液中,紫色溶液逐渐褪色 | |
| B. | 往氯化铁溶液中滴加氢氧化钠溶液,产生白色沉淀 | |
| C. | 将足量二氧化硫通入品红溶液中,红色溶液逐渐褪色 | |
| D. | 往葡萄糖溶液中加入新制氢氧化铜悬浊液并加热,产生红色沉淀 |
11.灰霾天气可以简洁地描述为是“细粒子气溶胶粒子在高湿度条件下引发的低能见度事件”.气溶胶是胶体的一种,关于胶体,下列说法不正确的是( )
| A. | 利用丁达尔现象可区别溶液和胶体 | |
| B. | 根据分散质和分散剂的状态,可以将胶体分为9种 | |
| C. | 气溶胶分散质粒子直径在1nm-100nm之间 | |
| D. | 向氢氧化钠溶液中边滴加饱和FeCl3溶液边震荡可制备Fe(OH)3胶体 |
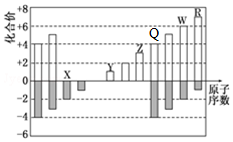 部分短周期元素化合价与原子序数的关系可用图表示.
部分短周期元素化合价与原子序数的关系可用图表示.