题目内容
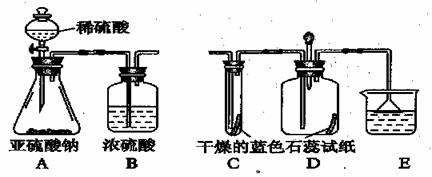
二氧化硫(SO2) 在通常情况下是一种无色刺激性气味的有毒气体,它能与氢氧化钠溶液反应,生成盐和水,现有某一实验小组的同学欲利用下图装置和药品制SO2 。并对SO2 与水在通常情况下能否反应,进行实验探究,设计的探究过程如下。请回答其中的有关问题:
(1)假设:SO2与水在通常情况下能反应,生成物是一种酸。
(2)设计方案:先验证水能否使蓝色石蕊试纸变红;再验证SO2 气体能否使干燥的蓝色石蕊试纸变色;最后验证SO2 气体能否便湿润的蓝色石蕊试纸变红。
(3)查阅资料:你认为该研究小组需要查阅的资料内容包括 。
①二氧化硫易溶于水;②酸能使紫色石蕊试纸变红; ③二氧化硫能用浓硫酸干燥。
(4)实验:①实验过程中;装置C 内的石蕊试纸的颜色始终没有变化,这说明
②装置D中胶头滴管中的蒸馏水在二氧化硫气体生成之前滴到蓝色石蕊试纸上,未见试纸发生颜色变化,当有SO2 气体通过时,发现湿润的蓝色石蕊试纸变化。此现象说明 __________________________________。
③装置E 的作用是 __,
写出发生反应的化学方程式 ________
(5) 结论:原假设 (填“成立”或“不成立”) 。
解析:设计方案中对照实验说明,使蓝色石蕊试纸变色的不是H2O ,也不是SO2 ,而是H2SO3 ,从而探究出SO2 在常温下可与H2O反应生成一种酸。
答案:(3) ①②③;
(4) ①说明:SO2 不会使干燥蓝色石蕊试纸变色;
②中说明:水不能使石蕊试纸变红,SO2与水共同存在下可使它变红;
③中E 的作用:防止水倒吸,SO2 + H2O= H2SO3 。
(5) 原假设成立

随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%。目前,消除大气污染有多种方法。
(1) 用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g) =4NO(g) + CO2(g) +2H2O(g) ⊿H= -574 kJ·mol-1
②CH4(g) +4NO(g) =2N2(g) + CO2(g) + 2H2O(g) ⊿H= -1160 kJ·mol-1
③H2O(g) = H2O(l) △H= -44.0 kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2 (g)、CO2 (g)和H2O(1)的热化学方程式 。
(2)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理。已知含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ = 4Fe3+ + 2H2O,则另一反应的离子方程式为 。
(3)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g) N2
(g)+CO2 (g) 。某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2
(g)+CO2 (g) 。某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
|
|
NO |
N2 |
CO2 |
|
0 |
1.00 |
0 |
0 |
|
10 |
0.58 |
0.21 |
0.21 |
|
20 |
0.40 |
0.30 |
0.30 |
|
30 |
0.40 |
0.30 |
0.30 |
|
40 |
0.32 |
0.34 |
0.17 |
|
50 |
0.32 |
0.34 |
0.17 |
①10min~20min以v(CO2) 表示的反应速率为 。
②根据表中数据,计算T1℃时该反应的平衡常数为 (保留两位小数)。
③一定温度下,随着NO的起始浓度增大,则NO的平衡转化率 (填“增大”、“不变”或“减小”) 。
④下列各项能作为判断该反应达到平衡的是 (填序号字母)。
A.容器内压强保持不变 B. 2v正(NO) = v逆(N2)
C.容器内CO2的体积分数不变 D.混合气体的密度保持不变
⑤30min末改变某一条件,过一段时间反应重新达到平衡,则改变的条件可能是 。请在下图中画出30min至40min 的变化曲线。

 N2(g)+2CO2(g)
△H<0。
N2(g)+2CO2(g)
△H<0。 
 浓度/mol·L-1
浓度/mol·L-1 时间/min
时间/min