题目内容
2.7克金属铝与足量氢氧化钠溶液反应,在标准状况下,生成气体的体积为多少升?
考点:化学方程式的有关计算
专题:计算题
分析:n(Al)=
=0.1mol,铝和氢氧化钠溶液反应方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑,根据方程式即可计算生成氢气的体积.
| 2.7g |
| 27g/mol |
解答:
解:n(Al)=
=
=0.1mol,铝和氢氧化钠溶液反应方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑,根据方程式知,
2Al+2H2O+2NaOH=2NaAlO2+3H2↑,
2mol 3mol
0.1mol n(H2)
n(H2)=0.15mol
氢气体积V(H2)=n×Vm=0.15mol×22.4L/mol=3.36L,
答:在标准状况下,生成气体的体积为3.36L.
| m |
| M |
| 2.7g |
| 27g/mol |
2Al+2H2O+2NaOH=2NaAlO2+3H2↑,
2mol 3mol
0.1mol n(H2)
n(H2)=0.15mol
氢气体积V(H2)=n×Vm=0.15mol×22.4L/mol=3.36L,
答:在标准状况下,生成气体的体积为3.36L.
点评:本题考查了根据方程式进行计算,掌握2Al+2H2O+2NaOH=2NaAlO2+3H2↑为解答关键,题目难度不大.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
下面关于硅的叙述中,正确的是( )
| A、硅的化学性质不活泼,常温下不与任何物质反应 |
| B、硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位 |
| C、硅的化学性质不活泼,在自然界中可以以游离态存在 |
| D、硅在电子工业中,是重要的半导体材料 |
对于方程Al2O3+N2+3C=2AlN+3CO下列说法正确的是( )
| A、Al2O3做氧化剂 |
| B、N2是还原剂 |
| C、AlN既是氧化产物又是还原产物 |
| D、若有1mol CO生成,则反应中有2mol电子转移 |
下列离子方程式与所述事实相符且正确的是( )
| A、漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- |
| B、Ca(HCO3)2溶液中加入足量NaOH溶液:HCO3-+OH-=H2O+CO32- |
| C、向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
| D、氢氧化钙溶液与碳酸氢镁溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
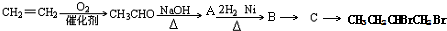
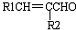 +H2O(-R1、R2表示氢原子或烃基)
+H2O(-R1、R2表示氢原子或烃基)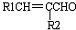
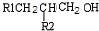
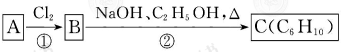
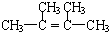 ;
;