题目内容
3.下列离子方程式正确的是( )| A. | 铁与稀硫酸反应:Fe+2H+═Fe3++H2↑ | |
| B. | 氢氧化铝与足量盐酸反应:Al(OH)3+3H+═Al3++3H2O | |
| C. | 钠和冷水反应:Na+2H2O═Na++H2↑+OH- | |
| D. | 过量二氧化碳与苛性钾反应:CO2+2OH-═CO32-+H2O |
分析 A.铁与稀硫酸反应生成硫酸亚铁和氢气;
B.氢氧化铝与稀盐酸反应生成氯化铝和水;
C.2mol钠与水反应生成1mol氢气,该反应不满足电子守恒;
D.二氧化碳过量,反应生成碳酸氢根离子.
解答 解:A.铁与稀硫酸反应生成氯化亚铁和氢气,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故A错误;
B.氢氧化铝与足量盐酸反应生成氯化铝和水,反应的离子方程式为:Al(OH)3+3H+═Al3++3H2O,故B正确;
C.钠和冷水反应生成氢氧化钠和氢气,正确的离子方程式为:2Na+2H2O═2Na++H2↑+2OH-,故C错误;
D.二氧化碳过量,反应生成的是碳酸氢根离子,正确的离子方程式为:CO2+OH-═HCO3-,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
14.下列说法正确的是( )
| A. | 同系物不一定符合同一通式 | |
| B. | 同分异构体不一定具有相同的最简式 | |
| C. | 相对分子质量相等的两种有机物必定是同分异构体 | |
| D. | 同分异构体间不一定有相似的化学性质 |
11.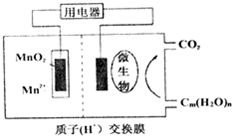 关于如图微生物燃料电池结构示意图的说法:
关于如图微生物燃料电池结构示意图的说法:
①微生物促进了电子的转移
②微生物所在电极区放电时发生还原反应
③放电过程中,H从正极区移向负极区
④正极反应式为:MnO2+4H++2e-═Mn2++2H2O
正确的是( )
 关于如图微生物燃料电池结构示意图的说法:
关于如图微生物燃料电池结构示意图的说法:①微生物促进了电子的转移
②微生物所在电极区放电时发生还原反应
③放电过程中,H从正极区移向负极区
④正极反应式为:MnO2+4H++2e-═Mn2++2H2O
正确的是( )
| A. | ④ | B. | ①③ | C. | ①④ | D. | ②③ |
8.下列关于浓硫酸的叙述正确的是( )
| A. | 浓硫酸具有吸水性,因而能使蔗糖炭化 | |
| B. | 浓硫酸常温下可与铜片迅速反应生成二氧化硫气体 | |
| C. | 浓硫酸是一种常用的干燥剂,可用来干燥氢气、氨气等 | |
| D. | 浓硫酸具有强氧化性,常温时可使铁、铝钝化 |
15.实验过程中如果浓苯酚溶液溅到皮肤上,紧急处理时最好采用的清洗液是( )
| A. | 用水冲洗 | B. | 用酒精洗 | C. | 用苯洗 | D. | 用NaOH溶液洗 |
12.有下列几种有机物,按照要求回答问题:
(1)A表示的分子式是C4H7Cl;所含官能团的名称是氯原子、碳碳双键.
(2)B可能发生的反应有①②③④(填序号).
①取代反应 ②消去反应 ③水解反应 ④酯化反应
(3)将B与氢氧化钠的乙醇溶液混合并加热,得到的主要产物发生加聚发生加聚反应生成聚合物的结构简式是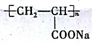 .
.
(4)有机物D是C的同分异构体,分子为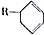 结构,D可能的结构有4种;写出
结构,D可能的结构有4种;写出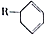 和Cl2发生1,4-加成反应的化学方程式:
和Cl2发生1,4-加成反应的化学方程式: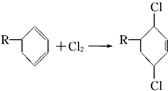 .
.
| A | B | C |
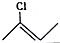 |  |  |
(2)B可能发生的反应有①②③④(填序号).
①取代反应 ②消去反应 ③水解反应 ④酯化反应
(3)将B与氢氧化钠的乙醇溶液混合并加热,得到的主要产物发生加聚发生加聚反应生成聚合物的结构简式是
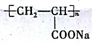 .
.(4)有机物D是C的同分异构体,分子为
 结构,D可能的结构有4种;写出
结构,D可能的结构有4种;写出 和Cl2发生1,4-加成反应的化学方程式:
和Cl2发生1,4-加成反应的化学方程式: .
.
13.H2CO3和 H2C2O4都是二元弱酸,不同 pH 环境下它们不同形态的粒子的组成百分率如图所示:

下列说法正确的是( )

下列说法正确的是( )
| A. | 在 pH 为 6.37 及 10.25 时,溶液中 c(H2CO3)=c(HCO3-)=c(CO32-) | |
| B. | 反应 HCO3-+H2O?H2CO3+OH-的平衡常数为 10-7.63 | |
| C. | 0.1 mol•L-1NaHC2O4溶液中 c(HC2O4-)+2c(C2O42-)+c(H2C2O4)=0.1 mol•L-1 | |
| D. | 往 Na2CO3溶液中加入少量草酸溶液,发生反应:CO32-+H2C2O4=HCO3-+HC2O4- |