题目内容
 铝及铝合金经过阳极氧化,铝表面能生成几十微米厚的氧化铝膜.某研究性学习小组模拟工业法对铝片表面进行氧化处理.分别以铅片、铝片为电极,以硫酸溶液为电解液,按照如图所示装置连接电解池装置,电解40min后取出铝片,用水冲洗,放在水蒸气中封闭处理20~30min,即可得到更加致密的氧化膜.下列有关说法正确的是( )
铝及铝合金经过阳极氧化,铝表面能生成几十微米厚的氧化铝膜.某研究性学习小组模拟工业法对铝片表面进行氧化处理.分别以铅片、铝片为电极,以硫酸溶液为电解液,按照如图所示装置连接电解池装置,电解40min后取出铝片,用水冲洗,放在水蒸气中封闭处理20~30min,即可得到更加致密的氧化膜.下列有关说法正确的是( )| A、电解时电子从电源负极→导线→铝极,铅极→导线→电源正级 |
| B、在电解过程中,H+向阳极移动,SO42-向阴极移动 |
| C、电解过程阳极周围溶液的pH下降 |
| D、电解的总反应为2Al+6H+═2Al3++3H2↑ |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、电解时电流从电源正极→负极,电流流向和电子流向相反;
B、在电解过程中,阳离子向阴极移动,阴离子向阳极移动;
C、电解时,阳极是活泼电极时,放电的是电极本身;
D、根据电解池的两极反应来分析电解的总反应.
B、在电解过程中,阳离子向阴极移动,阴离子向阳极移动;
C、电解时,阳极是活泼电极时,放电的是电极本身;
D、根据电解池的两极反应来分析电解的总反应.
解答:
解:A、电子流向和电流流向相反,电解时电子从电源负极→导线→铅极,铝极→导线→电源正极,故A错误;
B、在电解过程中,硫酸中的氢离子向阴极移动,硫酸根离子向阳极移动,故B错误;
C、电解时,阳极是活泼金属铝电极时,放电的是电极本身,pH基本不变,故C错误;
D、阳极是活泼金属铝电极,金属铝在该极失电子,阴极是氢离子得电子,所以电解的总方程式可表示为:2Al+6H+
2Al3++3H2↑,故D正确.
故选D.
B、在电解过程中,硫酸中的氢离子向阴极移动,硫酸根离子向阳极移动,故B错误;
C、电解时,阳极是活泼金属铝电极时,放电的是电极本身,pH基本不变,故C错误;
D、阳极是活泼金属铝电极,金属铝在该极失电子,阴极是氢离子得电子,所以电解的总方程式可表示为:2Al+6H+
| ||
故选D.
点评:本题是对电解原理的考查,可以根据所学知识进行回答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将0.39克锌粉加入到200ml 0.3mol/L的MO2+溶液中,恰好完全反应,则还原产物为( )
| A、M |
| B、M2+ |
| C、M3+ |
| D、MO2+ |
用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一种物质(括号内),溶液能与原来溶液完全一样的是( )
| A、CuCl2[Cu Cl2溶液] |
| B、NaOH[NaOH溶液] |
| C、NaCl[HCl气体] |
| D、CuSO4[Cu(OH)2] |
已知四种盐的溶解度(S)曲线如图所示,下列说法不正确的是( )


| A、将NaCl溶液蒸干可得NaCl固体 |
| B、将MgCl2溶液蒸干可得MgCl2固体 |
| C、可用MgCl2和NaClO3制备Mg(ClO3)2 |
| D、Mg(ClO3)2中混有少量NaCl杂质,可用重结晶法提纯 |
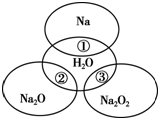 如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )
如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )| A、Na2O2中阴阳离子数目之比为1:1 |
| B、反应①的离子方程式为Na+2H2O═Na++2OH-+H2↑ |
| C、反应③最多能转移0.1 mol电子 |
| D、①、②、③充分反应后所得溶液中溶质的质量分数:①>②>③ |
能使0.1mol/LCH3COONa溶液的pH值增大的方法是( )
| A、加水 | B、加盐酸 |
| C、加热 | D、加氯化铵晶体 |
 (X为卤原子)
(X为卤原子)