题目内容
11.常温时,将CH3COOH溶液和NaOH溶液等体积混合后,溶液呈中性,下列各项可能正确的是( )| A. | 混合前pH(CH3COOH)+pH(NaOH)=14 | B. | 混合后c(Na+)=c(CH3COO3-)+c(OH-) | ||
| C. | 混合前c(CH3COOH)>c(NaOH) | D. | 混合后c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
分析 醋酸为弱酸,如二者恰好反应,溶液呈碱性,将CH3COOH溶液和NaOH溶液等体积混合后,溶液呈中性,醋酸应过量,即醋酸的浓度大于NaOH浓度,结合溶液的电中性原则解答该题.
解答 解:A.混合前pH(CH3COOH)+pH(NaOH)=14,则应有c(OH-)=c(H+),醋酸部分电离,所以醋酸的浓度大于氢离子浓度,二者混合醋酸过量,溶液显酸性,故A错误;
B.溶液中电荷守恒为c(Na+)+c(H+)=c(CH3COO-)+c(OH-),所以c(Na+)<c(CH3COO3-)+c(OH-),故B错误;
C.醋酸为弱酸,如c(CH3COOH)=c(NaOH),二者恰好反应,溶液呈碱性,溶液呈中性,醋酸应过量,即混合前:c(CH3COOH)>c(NaOH),故C正确;
D.溶液呈中性,由电荷守恒c(Na+)+c(H+)=c(CH3COO-)+c(OH-)可知,应存在c(Na+)=c(CH3COO-)>c(OH-)=c(H+),故D错误.
故选C.
点评 本题考查酸碱混合的定性判断和离子浓度的大小比较,题目难度中等,本题易错点为A,注意pH(CH3COOH)+pH(NaOH)=14,酸碱溶液中存在c(OH-)=c(H+),醋酸过量,溶液呈酸性.

练习册系列答案
相关题目
16.室温下,将0.4mol/L一元酸HA溶液和0.2mol/LNaOH溶液等体积混合(忽略混合时溶液体积的变化),测得混合液的pH=5,则下列说法或粒子浓度关系式正确的是( )
| A. | 混合液中由水电离出的c(H+)=1×10-8mol/L | |
| B. | c(A-)+c(HA)=2c(Na+)=0.4mol/L | |
| C. | HA溶液中$\frac{c({A}^{-})}{c(HA)•c(O{H}^{-})}$与混合液中$\frac{c({A}^{-})}{c(HA)•c(O{H}^{-})}$相等 | |
| D. | c(A-)-c(HA)=2c(OH-)-2c(H+) |
3.25℃把 0.02mol/LCH3COOH溶液和0.01mol/LKOH溶液以等体积混和,则混合液中微粒浓度关系正确的为:(已知?25℃:CH3COOH电离常数是1.76×10-5,CH3COO-水解常数是5.78×10-10;?体积变化忽略不计;)( )
| A. | c (K+)>c (CH3COO-)>c(H+)>c (OH-) | B. | c(K+)=c (CH3COO-)>c (OH-)=c (H+) | ||
| C. | c(K+)+c (H+)═c(CH3COOH)+c (OH-) | D. | c (CH3COOH)+c (CH3COO-)=0.01mol/L |
1.科学家在研究化学物质吋,常常对物质逬行分类,以便对同类物质的组成和性质进行深人的研究,下列4组物质:
①Ca、S、Cl2、NO2②NH3•H2O、Na2CO3、CH4、KCl③H2CO3、H2SO4、NaOH、H2SiO3④MgO、SO2、CO2、SiO2从物质的基本分类看,每组中都有一种物质与其它物质不属于同这4种物质分别是( )
①Ca、S、Cl2、NO2②NH3•H2O、Na2CO3、CH4、KCl③H2CO3、H2SO4、NaOH、H2SiO3④MgO、SO2、CO2、SiO2从物质的基本分类看,每组中都有一种物质与其它物质不属于同这4种物质分别是( )
| A. | NO2、CH4、NaOH、MgO | B. | Cl2、NH3•H20、NaOH、Si02 | ||
| C. | Ca、Ma2C03、H2Si03、MgO | D. | NO2、CH4、H2SiO3、SO2 |
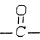 ,则A的可能结构式为
,则A的可能结构式为 、CH3CH2CHO;
、CH3CH2CHO; 实验室要配制2mol/L稀硫酸250mL.
实验室要配制2mol/L稀硫酸250mL.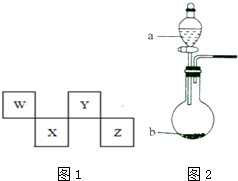 W、X、Y、Z四种短周期元素在周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物.
W、X、Y、Z四种短周期元素在周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物.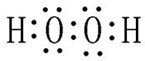 ,Z在周期表中的位置第三周期ⅦA族.
,Z在周期表中的位置第三周期ⅦA族.