题目内容
下列各组离子,在强碱性溶液中可以大量共存的是( )
A、Cl-、NO
| ||||
B、K+、AlO
| ||||
| C、Br-、S2-、Cl-、Mg2+ | ||||
D、Na+、I-、NH
|
考点:离子共存问题
专题:离子反应专题
分析:强碱性溶液中,含大量的OH-,根据离子之间不能结合生成沉淀、气体、水、弱电解质等,则离子大量共存,以此来解答.
解答:
解:A.OH-、Ca2+、HCO3-发生反应生成CaCO3沉淀而不能大量共存,故A错误;
B.碱性条件下离子之间不发生任何反应,可大量共存,故B正确;
C.碱性条件下Mg2+不能大量共存,故C错误;
D.碱性条件下,NH4+不能大量共存,故D错误.
故选B.
B.碱性条件下离子之间不发生任何反应,可大量共存,故B正确;
C.碱性条件下Mg2+不能大量共存,故C错误;
D.碱性条件下,NH4+不能大量共存,故D错误.
故选B.
点评:本题考查离子共存问题,为高考常见题型和高频考点,答题时注意题目碱性以及可以大量共存的要求,注意相关离子的性质以及反应类型的判断,难度不大.

练习册系列答案
相关题目
在某密闭恒容容器中存在下列化学平衡:aA(气)?bB(气)+cC(气),在温度不变的条件下,再充入一定量的A物质,重新达到平衡时,下列判断中正确的是( )
| A、若 a=b+c,B的物质的量分数变大 |
| B、若 a>b+c,B 的物质的量分数减小 |
| C、若a>b+c时,A的转化率不变 |
| D、若a<b+c时,A的转化率变小 |
下列混合物的分离和提纯方法中,主要是从物质沸点的角度考虑的是( )
| A、蒸发 | B、蒸馏 | C、过滤 | D、萃取 |
想一想:NaOH(固体)、FeSO4(固体)、HCl(液态)这些物质为什么归为一类,下列哪些物质还可以和它们归为一类( )
| A、75%的酒精溶液 |
| B、硝酸钠 |
| C、Fe(OH)3胶体溶液 |
| D、豆浆 |
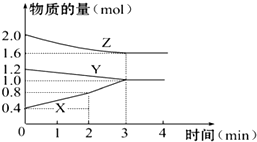 某温度时,在容积为3L的密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示,由图中数据分析正确的是( )
某温度时,在容积为3L的密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示,由图中数据分析正确的是( )| A、该反应的化学方程式为Y+2Z=3X |
| B、反应开始至2 min时,X的逆反应速率要大于正反应速率 |
| C、该反应是由正、逆反应同时开始的 |
| D、若增加Y的用量,化学反应速率不变化,则Y一定为固态 |
不能用磨口玻璃塞的试剂瓶盛装的溶液是( )
| A、硫酸铜 | B、氢氧化钠 |
| C、硝酸银 | D、氯化钠 |
常温下,下列各组离子一定能大量共存的是( )
| A、甲基橙变红的溶液中:Cu2+、Al3+、NO3-、I- |
| B、氢氧化铁胶体中:H+、K+、SO42-、Br- |
| C、含有大量的CO32-溶液中:NH4+、Na+、SO42-、Cl- |
| D、c(Al3+)=0.1 mol?L-1的溶液中:Na+、Cl-、HCO3-、SO42- |
一定条件下,体积为10L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g)?Z(g),经60s达到平衡,生成0.3molZ.下列说法正确的是( )
| A、反应进行30s时,正反应速率大于逆反应速率 |
| B、反应进行80s时,逆反应速率大于正反应速率 |
| C、反应进行60s时,此时v(X)为0.001mol/(L?s),且保持不变 |
| D、反应进行80s时,X物质的量浓度为0.04mol/L |