题目内容
18.在一定温度下,将200g硫酸钠溶液与100g氯化钡溶液混合,恰好完全反应.过滤得到滤液276.7g,往滤液中加入83.7g该滤液的溶质并恢复到原温度,溶液恰好饱和.求:
(1)原硫酸钠溶液中溶质的质量.
(2)滤液中的溶质在该温度下的溶解度为多少?
分析 混合发生反应:Na2SO4+BaCl2═BaSO4↓+2NaCl,生成沉淀为硫酸钡,则硫酸钡沉淀的质量=200g+100g-276.7g=23.3g,根据硫酸钡质量计算硫酸钠、生成氯化钠的质量,根据饱和溶液质量分数w=$\frac{s}{s+100}$计算NaCl的溶解度.
解答 解:(1)硫酸钡沉淀的质量=200g+100g-276.7g=23.3g,
设硫酸钠的质量为x,反应生成的氯化钠的质量为y
Na2SO4+BaCl2═BaSO4↓+2NaCl
142 233 117
x 23.3g y
所以x=$\frac{23.3g×142}{233}$=14.2g
y=$\frac{23.3g×117}{233}$=11.7g
(2)滤液中的溶质在该温度下的溶解度s,则$\frac{s}{100g+s}$=$\frac{11.7g+83.7g}{276.7g+83.7g}$,解得s=36g
答:(1)原硫酸钠溶液中溶质的质量为14.2g;
(2)滤液中的溶质在该温度下的溶解度为36g.
点评 本题考查混合物有关计算、溶解度计算,明确发生的反应即可解答,注意对溶解度的理解掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.青蒿素对治疗疟疾有很好的效果,下列说法正确的是( )


| A. | 青蒿素易溶于水和酒精 | |
| B. | 青蒿素中含多个环状结构,其中有一个六元碳环 | |
| C. | 青蒿素中含过氧键,过氧键属于极性共价键 | |
| D. | 青蒿素和纤维素都属于高分子化合物 |
9.下列事实不能说明醋酸属于弱电解质的是( )
| A. | 0.1mol/L CH3COONa溶液显碱性 | |
| B. | 0.1mol/L醋酸溶液的pH=3 | |
| C. | 物质的量浓度相同的盐酸和醋酸同时与锌反应,开始时锌粒跟盐酸反应比跟醋酸反应的速率快 | |
| D. | 中和100mL1mol/L 的CH3COOH溶液需要100mL1mol/L的NaOH溶液 |
6.已知32g X与40g Y恰好完全反应,生成m g Q和9g H,在相同条件下,16g X和足量Y混合生成0.25mol Q和若干摩的H,则物质Q的摩尔质量应是( )
| A. | 122 g•mol-1 | B. | 63 g•mol-1 | C. | 126 g•mol-1 | D. | 163 g•mol-1 |
13.“学做营养师,我来配食谱.”我们来帮小明同学完成下列食谱.
除了水和无机盐之外,上表食谱中,含有的营养素主要有糖类、蛋白质(或油脂)等(写两种);我认为小明列出的食谱中还缺少一种人体所必需的营养素维生素,“我的补充”是青菜(填写获取该营养素的一种食物名称).
| 主食 | 米饭 | 馒头 | ||
| 副食 | 烧鱼块 | 咸鸡蛋 | 红烧肉 | 花生米 |
| 饮料 | 牛奶 | |||
| 我的 |
10.下列各项叙述中,正确的是( )
| A. | 镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 | |
| B. | 第一电离能由小到大的顺序是S<P<Cl | |
| C. | 47Ag原子的价层电子排布式是4d95s2 | |
| D. | 价电子排布为5s25p1的元素位于第五周期第ⅠA族,是p区元素 |
7.二氧化锰是制造锌锰干电池的基本材料.工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如图1:
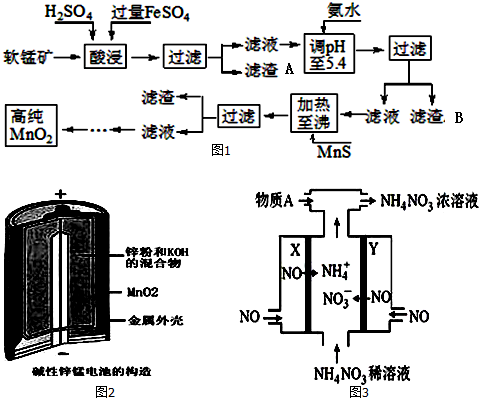
某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH如表,回答下列问题
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为MnO2+2FeSO4+2H2SO4═MnSO4+Fe2(SO4)3+2H2O.
(2)滤渣A的主要成分是SiO2;滤渣B的主要成分是Fe(OH)3、Al(OH)3.
(3)加入MnS的目的是除去Cu2+、Zn2+杂质.可能原因是CuS、ZnS的溶解度较MnS小.
(4)碱性锌锰电池是一种一次性电池,其结构如图2所示.该电池放电过程产生MnOOH.该电池的正极反应式为MnO2+H2O+e-═MnO(OH)+OH-,电池总反应的方程式为Zn+2MnO2+2H2O═2MnOOH+ZnOH)2.
(5)利用该碱性锌锰电池电解NO制备NH4NO3,其工作原理如图3所示,X电极阴极,电解时阳极的电极反应为NO-3e-+2H2O=NO3-+4H+,使电解产物全部转化为NH4NO3,需补充物质A,A是NH3.

某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH如表,回答下列问题
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ≥-0.42 | ≥2.5 | ≥7 | ≥7 |
(2)滤渣A的主要成分是SiO2;滤渣B的主要成分是Fe(OH)3、Al(OH)3.
(3)加入MnS的目的是除去Cu2+、Zn2+杂质.可能原因是CuS、ZnS的溶解度较MnS小.
(4)碱性锌锰电池是一种一次性电池,其结构如图2所示.该电池放电过程产生MnOOH.该电池的正极反应式为MnO2+H2O+e-═MnO(OH)+OH-,电池总反应的方程式为Zn+2MnO2+2H2O═2MnOOH+ZnOH)2.
(5)利用该碱性锌锰电池电解NO制备NH4NO3,其工作原理如图3所示,X电极阴极,电解时阳极的电极反应为NO-3e-+2H2O=NO3-+4H+,使电解产物全部转化为NH4NO3,需补充物质A,A是NH3.
8.关于化学平衡常数的叙述正确的是( )
| A. | 温度一定,一个化学反应的平衡常数是一个常数 | |
| B. | 两种物质反应,不管怎样书写化学方程式,平衡常数不变 | |
| C. | 温度一定时,对于给定的化学反应,正、逆反应的平衡常数互为倒数 | |
| D. | 浓度商Qc<Kc,v(正)<v(逆) |