题目内容
下列说法正确的是( )
| A、摩尔是把物质的质量和微观粒子数联系起来的一个基本物理量 |
| B、摩尔是国际单位制中七个基本物理量之一 |
| C、1摩尔氢气分子可以表示为1molH2 |
| D、国际上规定,0.012 kg 碳原子所含有的碳原子数目为1摩尔 |
考点:物质的量的单位--摩尔
专题:化学用语专题
分析:A、摩尔是物质的量的单位;
B、摩尔是物质的量的单位;
C、物质的量适用微观粒子;
D、根据阿伏伽德罗常数的定义分析.
B、摩尔是物质的量的单位;
C、物质的量适用微观粒子;
D、根据阿伏伽德罗常数的定义分析.
解答:
解:A、摩尔是物质的量的单位,不是基本物理量,故A错误;
B、摩尔是物质的量的单位,不是基本物理量,物质的量是国际单位制中七个基本物理量之一,故B错误;
C、物质的量适用微观粒子,1摩尔氢气分子可以表示为1molH2,故C正确;
D、国际上规定,0.012 kg 碳原子所含有的碳原子数目为摩尔阿伏伽德罗常数,故D错误.
故选C.
B、摩尔是物质的量的单位,不是基本物理量,物质的量是国际单位制中七个基本物理量之一,故B错误;
C、物质的量适用微观粒子,1摩尔氢气分子可以表示为1molH2,故C正确;
D、国际上规定,0.012 kg 碳原子所含有的碳原子数目为摩尔阿伏伽德罗常数,故D错误.
故选C.
点评:本题考查了物质的量及其单位的含义、阿伏伽德罗常数,题目比较简单,侧重于对基本概念的考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
现有三组溶液:①氯化钠和单质溴的水溶液 ②汽油和氯化钠溶液③19%的乙醇溶液,分离以上各混合液的正确方法依次是( )
| A、.萃取、分液、蒸馏 |
| B、分液、萃取、蒸馏 |
| C、萃取、蒸馏、分液 |
| D、蒸馏、分液、萃取 |
某工业生产经过以下转化步骤:
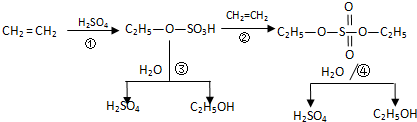
下列说法中不正确的是( )

下列说法中不正确的是( )
| A、该过程中③、④是酯类的水解反应 |
| B、该过程中硫酸是催化剂 |
| C、该过程中①、②是加成反应 |
| D、该过程是一种新的硫酸生产方法 |
下列物质所属的类别及其所含官能团的对应关系错误的是( )
A、CH3CH=CH2 烯烃  |
B、 醛类-CHO 醛类-CHO |
C、 羧酸-COOH 羧酸-COOH |
| D、RCH2OH(R,烃基) 醇类-OH |
下列说法正确的是(NA表示阿伏加德罗常数的数值)( )
| A、在常温常压下,11.2 L N2含有的分子数为0.5 NA |
| B、22.4L Cl2所含原子数为2NA |
| C、在常温常压下,1 mol Ne含有的原子数为NA |
| D、在同温同压时,相同体积的任何气体单质所含的原子数相同 |
下列反应为氧化还原反应的是( )
| A、HCl+NaOH═NaCl+H2O |
| B、2H2+O2═2H2O |
| C、CaO+H2O═Ca(OH)2 |
| D、CaCO3═CaO+CO2 |
短周期元素X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为14;X原子的内层电子数与Y原子的最外层电子数相等;X原子的核外电子总数与Z原子的最外层电子数相等.下列说法正确的是( )
| A、X的氧化物都能与水反应生成酸 |
| B、Z的离子半径比Y的离子半径小 |
| C、Y和Z组成的化合物是离子化合物 |
| D、X的气态氢化物分子与Z的离子具有相同的电子数 |
N2H4是常用的火箭高能燃料,与H2O2混合可做液体推进剂,反应为:N2H4+2H2O2═N2+4H2O,下列有关说法中正确的是( )
| A、N2H4分子中既存在极性键,又存在离子键 |
B、H2O2分子的电子式为: |
| C、28g N2中含有π键数目为2NA |
D、水分子的球棍模型 |
某化合物6.4g完全燃烧,只生成8.8克CO2和7.2克H2O.下列说法正确的是( )
| A、该化合物仅含碳、氢两种元素 |
| B、无法确定该化合物是否含有氧无素 |
| C、该化合物中一定含有氧元素 |
| D、该化合物中碳、氢原子个数比为1:2 |