题目内容
将0.05molBa(OH)2固体分别加入500mL下列液体中,溶液的导电能力变化最小的是( )
| A、自来水 |
| B、0.1mol?L-1的硫酸 |
| C、0.2mol?L-1的醋酸 |
| D、0.2mol?L-1的Na2CO3溶液 |
考点:电解质溶液的导电性,电解质在水溶液中的电离
专题:离子反应专题
分析:溶液混合后导电能力变化的大小,关键是看混合后溶液中自由移动的离子浓度的变化,根据物质之间的反应判断,如果离子浓度增大或减少很多,故导电能力与原来相比变化很大.
解答:
解:A、因水是极弱的电解质,导电性极弱,加入Ba(OH)2固体,Ba(OH)2是强电解质,溶液中主要的是钡离子和氢氧根,导电性增强,故A不选;
B、0.1mol?L-1的硫酸中加入少量Ba(OH)2固体反应生成的是水和硫酸钡沉淀,反应过程中离子浓度明显减小,溶液的导电能力变化很明显,故B不选;
C、0.2mol?L-1的醋酸,醋酸是弱电解质,离子较少,加入强碱以后,变为强电解质,导电能力增强,故C不选;
D、0.2mol?L-1的Na2CO3溶液,加入Ba(OH)2固体生成碳酸钡沉淀和氢氧化钠,溶液中离子所带电荷的浓度变化不大,故导电性变化不大,故D选;
故选D.
B、0.1mol?L-1的硫酸中加入少量Ba(OH)2固体反应生成的是水和硫酸钡沉淀,反应过程中离子浓度明显减小,溶液的导电能力变化很明显,故B不选;
C、0.2mol?L-1的醋酸,醋酸是弱电解质,离子较少,加入强碱以后,变为强电解质,导电能力增强,故C不选;
D、0.2mol?L-1的Na2CO3溶液,加入Ba(OH)2固体生成碳酸钡沉淀和氢氧化钠,溶液中离子所带电荷的浓度变化不大,故导电性变化不大,故D选;
故选D.
点评:本题考查溶液中离子浓度大小比较,以此判断溶液的导电性,溶液混合后导电能力变化的大小,关键是看混合后溶液中自由移动的离子浓度的变化,题目难度不大.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
用惰性电极电解足量的下列溶液,一段时间后,加入一定质量的另一种物质(中括号内),溶液能与原来溶液完全一样的是( )
| A、CuCl2[CuSO4] |
| B、NaOH[H2O] |
| C、NaCl[H2O] |
| D、CuSO4[Cu(OH)2] |
分别将一小块钠投入下列溶液中,只有一种气体放出,没有沉淀生成的是( )
| A、饱和NaCl溶液 |
| B、稀NaHSO4溶液 |
| C、MgCl2溶液 |
| D、CuSO4溶液 |
在无色透明溶液中,下列各离子组能大量共存的是( )
| A、SO42- Na+Fe3+ Cl- |
| B、Ba2+ Na+Cl- SO42- |
| C、HCO3-K+ SO42-OH- |
| D、Ag+ Al3+ NO3-H+ |
下列物质属于电解质且又能导电的是( )
| A、硝酸钾溶液 |
| B、液态的氯化氢 |
| C、熔融的氯化钠 |
| D、金属铜 |
对于可逆反应H2(g)+I2(g)?2HI(g),在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是( )
| A、H2(g)的消耗速率与HI(g)的生成速率之比为2:1 |
| B、正、逆反应速率的比值是恒定的 |
| C、当HI的分子数与I2分子数之比为2:1时,说明反应达到了平衡状态 |
| D、达到平衡时,正、逆反应速率相等 |
下列变化中,能表明硝酸具有氧化性的是( )
| A、石蕊试剂变红色 |
| B、能跟Ag反应生成AgNO3 |
| C、碳酸钙反应 |
| D、能和FeO反应生成Fe(NO3)3 |
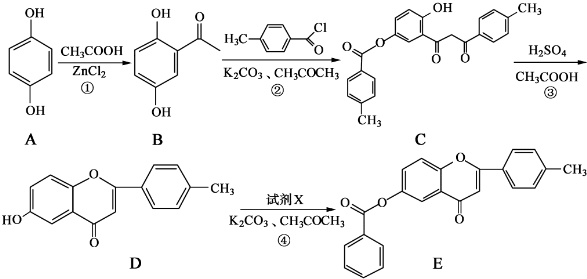

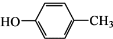 和CH3COOH为原料制备
和CH3COOH为原料制备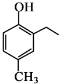 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: