��Ŀ����
9����1��X��Y��Z��Q��R�����ֶ�����Ԫ�أ�ԭ��������������X��ԭ�Ӱ뾶��С������Ԫ�أ�YԪ����������������֮��Ϊ0��Q��Xͬ���壬��Z��R�ֱ��ǵؿ��к�����ߵķǽ���Ԫ�غͽ���Ԫ�أ���ش��������⣺������Ԫ���У�ԭ�Ӱ뾶������Na���ǽ�������ǿ����O����дԪ�ط��ţ�
��X��Y���γɶ��ֻ�������мȺ����Լ��ֺ��Ǽ��Լ�������Է���������С�����ʣ�д����ʽ��C2H2
��������ijЩԪ����ɵĻ�����A��B��C��D������ת����ϵ��A$?_{D}^{C}$B����ˮ��Һ�н��У�����C������ˮ�����Ե����壻D�ǵ���ɫ���壮д��D�ĵ���ʽ
 �����A��B��������Ԫ����ɣ�BΪ���Բ��������A�������C��Ӧת��ΪB�����ӷ���ʽΪAlO2-+CO2+2H2O=Al��OH��3��+HCO3-��
�����A��B��������Ԫ����ɣ�BΪ���Բ��������A�������C��Ӧת��ΪB�����ӷ���ʽΪAlO2-+CO2+2H2O=Al��OH��3��+HCO3-����2����ҵ�ϳɰ�ʱ���ϳ�����ÿ����1mol NH3���ų�46.1kJ��������
�ٹ�ҵ�ϳɰ����Ȼ�ѧ����ʽ��N2��g��+3H2��g��?2NH3��g����H=-92.2kJ/mol��
����֪��N��N�ļ���Ϊ945.8kJ/mol��H-H�ļ���Ϊ436.0kJ/mol����Ͽ�1mol N-H�������������391kJ��
��3������һ��DZ�ڵ������Դ������������ȼ�ϵ�ص�ȼ�ϣ���ص��ܷ�ӦΪ��4NH3��g��+3O2��g���T2N2��g��+6H2O��g�������ȼ�ϵ�صĸ�����Ӧʽ��2NH3+6OH--6e-=N2+6H2O��
���� ��1��X��Y��Z��Q��R�����ֶ�����Ԫ�أ�ԭ��������������X��ԭ�Ӱ뾶��С������Ԫ�أ���XΪHԪ�أ�Z��R�ֱ��ǵؿ��к�����ߵķǽ���Ԫ�غͽ���Ԫ�أ���ZΪOԪ�ء�RΪAl��YԪ����������������֮��Ϊ0����ԭ��������֪��ֻ�ܴ��ڵڢ�A�壬����ԭ��������С��OԪ�أ���YΪ̼Ԫ�أ�Q��Xͬ���壬���ԭ��������֪QΪNa��
��2���ټ�������2mol�����ų���������ע�����ʵľۼ�״̬�뷴Ӧ����д�Ȼ�ѧ����ʽ��
�ڷ�Ӧ��=��Ӧ���ܼ���-�������ܼ��ܣ�
��3��ԭ��ظ�������������Ӧ�������ڸ���ʧȥ���ӣ��������������ɵ�����ˮ��
��� �⣺��1��X��Y��Z��Q��R�����ֶ�����Ԫ�أ�ԭ��������������X��ԭ�Ӱ뾶��С������Ԫ�أ���XΪHԪ�أ�Z��R�ֱ��ǵؿ��к�����ߵķǽ���Ԫ�غͽ���Ԫ�أ���ZΪOԪ�ء�RΪAl��YԪ����������������֮��Ϊ0����ԭ��������֪��ֻ�ܴ��ڵڢ�A�壬����ԭ��������С��OԪ�أ���YΪ̼Ԫ�أ�Q��Xͬ���壬���ԭ��������֪QΪNa��
������Ԫ����Hԭ�Ӱ뾶��С��ͬ�����������ԭ�Ӱ뾶��С���ǽ�����ǿ��ͬ�������϶���ԭ�Ӱ뾶���ǽ����Լ���������������Ԫ���У�Na��ԭ�Ӱ뾶���O�ķǽ�������ǿ��
�ʴ�Ϊ��Na��O��
��H��C���γɶ��ֻ�������мȺ����Լ��ֺ��Ǽ��Լ�������Է���������С������ΪC2H2��
�ʴ�Ϊ��C2H2��
��������ijЩԪ����ɵĻ�����A��B��C��D������ת����ϵ��A$?_{D}^{C}$B����ˮ��Һ�н��У�������C������ˮ�����Ե����壬��CΪCO2��D�ǵ���ɫ������DΪNa2O2��Na2O2�ĵ���ʽΪ ��
��
���A��B��������Ԫ����ɣ�BΪ���Ի�����Ҳ�����ˮ����BΪAl��OH��3��AΪNaAlO2�����������CO2��Ӧ����������������������̼�����ƣ���Ӧ���ӷ���ʽΪ��AlO2-+CO2+2H2O=Al��OH��3��+HCO3-��
�ʴ�Ϊ�� ��AlO2-+CO2+2H2O=Al��OH��3��+HCO3-��
��AlO2-+CO2+2H2O=Al��OH��3��+HCO3-��
��2��������2mol�����ų�������Ϊ46.1kJ��2=92.2kJ����Ӧ�Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��?2NH3��g����H=-92.2kJ/mol��
�ʴ�Ϊ��N2��g��+3H2��g��?2NH3��g����H=-92.2kJ/mol��
����Ͽ�1mol N-H�������������xkJ����945.8kJ/mol+3��436.0kJ/mol-6��xkJ/mol=-92.2kJ/mol�����x=391��
�ʴ�Ϊ��391��
��3��ԭ��ظ�������������Ӧ�������ڸ���ʧȥ���ӣ��������������ɵ�����ˮ�������缫��ӦʽΪ��2NH3+6OH--6e-=N2+6H2O��
�ʴ�Ϊ��2NH3+6OH--6e-=N2+6H2O��
���� ���⿼��ṹ����λ�ù�ϵӦ�á��Ȼ�ѧ����ʽ��д�������뷴Ӧ�ȹ�ϵ��ԭ��صȣ��ƶ�Ԫ���ǽ���Ĺؼ���ע��Ԫ����������������֮�;�Ϊ0������Ϊ��A��Ԫ�أ�Ҳ����ΪHԪ�أ���ѧ�н����漰HԪ�صĸ����ϼۣ�

| ���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
��2�����������У����������ˮ����������ǿ����HClO4���ѧʽ����
��3��C��N�У�ԭ�Ӱ뾶��С����N��
��4��Si�Ǵ���������������ҪԪ��֮һ���������ﳣ����������ά����һ�ָ����ܵ��ִ�ͨѶ���ϵ����ƣ���
��5��þ��һ����Ҫ�Ľ������ϣ���ҵ�ϲ��õ�������Ȼ�þ��ý���þ���÷�Ӧ�Ļ�ѧ����ʽΪMgCl2$\frac{\underline{\;���\;}}{\;}$Mg+Cl2����
| A�� | 35g | B�� | 30g | C�� | 20g | D�� | 15g |

| A�� | ԭ��ص��ܷ�ӦΪFe+Cu2+�TFe2++Cu | |
| B�� | ��������KNO3��Һ����������NO3-�������ձ� | |
| C�� | �����������䣬����CuCl2��Һ��ΪNH4Cl��Һ��ʯī�缫��ӦʽΪ2H++2e-�TH2�� | |
| D�� | ��Ӧǰ���缫������ȣ�һ��ʱ������缫�������12g��������ͨ��0.2mol���� |
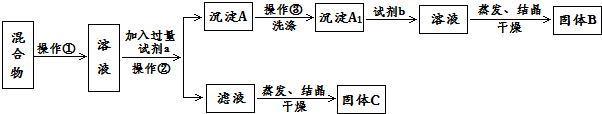
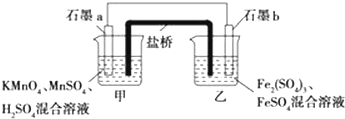
 ��
�� ��ͬʱ��������������B��ͬ���칹�壨������B������11�֣�����FeCl3��Һ����ɫ��������ֻ������ȡ������
��ͬʱ��������������B��ͬ���칹�壨������B������11�֣�����FeCl3��Һ����ɫ��������ֻ������ȡ������ ����дһ�֣���
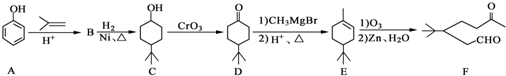
����дһ�֣���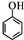 ����CH2=CH2Ϊԭ���Ʊ��л���
����CH2=CH2Ϊԭ���Ʊ��л���  �ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�
�ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�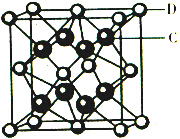 ��֪A��B��C��D��E����Ԫ�����ڱ���ǰ36�ŵ�Ԫ�أ����ǵ�ԭ��������������Aԭ�ӻ�̬ʱ���������������ڲ����������2����Bԭ�ӻ�̬ʱs��������P��������ȣ�C��Ԫ�����ڱ��ĸ�Ԫ���е縺�����D�Ļ�̬ԭ�Ӻ�����6���ܼ���ȫ���������ӣ�Eԭ�ӻ�̬ʱδ�ɶԵ�������ͬ����Ԫ�������ģ�Fԭ�Ӻ���������������Na��ͬ�����������Ӿ�������
��֪A��B��C��D��E����Ԫ�����ڱ���ǰ36�ŵ�Ԫ�أ����ǵ�ԭ��������������Aԭ�ӻ�̬ʱ���������������ڲ����������2����Bԭ�ӻ�̬ʱs��������P��������ȣ�C��Ԫ�����ڱ��ĸ�Ԫ���е縺�����D�Ļ�̬ԭ�Ӻ�����6���ܼ���ȫ���������ӣ�Eԭ�ӻ�̬ʱδ�ɶԵ�������ͬ����Ԫ�������ģ�Fԭ�Ӻ���������������Na��ͬ�����������Ӿ�������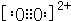 ��1mol B22+�к��еĦм���ĿΪ2NA��
��1mol B22+�к��еĦм���ĿΪ2NA�� �����ӻ����ᄃ����ܶ�Ϊa g/cm3�����������$\frac{312}{a{N}_{A}}$ cm3��ֻҪ������ʽ�������ӵ�������ֵΪNA����
�����ӻ����ᄃ����ܶ�Ϊa g/cm3�����������$\frac{312}{a{N}_{A}}$ cm3��ֻҪ������ʽ�������ӵ�������ֵΪNA����