题目内容
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最小;B元素的最高价氧化物对应水化物与其氢化物能生成盐M;D与A同主族,且与E同周期;E元素原子的最外层电子数比次外层电子数少2;A、B、D、E这四种元素,每一种与C元素都能形成原子个数比不相同的若干种化合物.请回答:
(1)C和E两种元素相比较,原子得电子能力较强的元素在周期表中的位置为 ,以下三种说法中,可以验证C和E得电子能力强弱的是(填写编号) ;
a.比较这两种元素的常见单质的沸点
b.二者形成的化合物中,C元素的原子显负价
c.比较这两种元素的气态氢化物的稳定性
(2)盐M中含有的化学键类型有 ;
(3)A、B、C、E可形成两种酸式盐(均含有该四种元素),这两种酸式盐在水溶液中相互反应的离子方程式为 .
(4)B2A4是一种可燃性液体,B2A4-空气燃料电池是一种碱性燃料电池,B2A4的氧化产物为B2.则负极上的电极反应式为 .
(5)已知1molD与水反应放出283.5kJ的热量,试写出D与水反应的热化学反应方程式 .
(1)C和E两种元素相比较,原子得电子能力较强的元素在周期表中的位置为
a.比较这两种元素的常见单质的沸点
b.二者形成的化合物中,C元素的原子显负价
c.比较这两种元素的气态氢化物的稳定性
(2)盐M中含有的化学键类型有
(3)A、B、C、E可形成两种酸式盐(均含有该四种元素),这两种酸式盐在水溶液中相互反应的离子方程式为
(4)B2A4是一种可燃性液体,B2A4-空气燃料电池是一种碱性燃料电池,B2A4的氧化产物为B2.则负极上的电极反应式为
(5)已知1molD与水反应放出283.5kJ的热量,试写出D与水反应的热化学反应方程式
考点:位置结构性质的相互关系应用
专题:
分析:A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最小,所以A是H元素;B元素的最高价氧化物对应水化物与其氢化物能生成盐M,所以B是N元素;D与A同主族,且与E同周期;E元素原子的最外层电子数比次外层电子数少2,且是短周期元素,所以E是S元素,则D是Na元素;A、B、D、E这四种元素,每一种与C元素都能形成原子个数比不相同的若干种化合物,所以C是O元素,据此结合各元素及其化合物的性质解答.
解答:
解:A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最小,所以A是H元素;B元素的最高价氧化物对应水化物与其氢化物能生成盐M,所以B是N元素;D与A同主族,且与E同周期;E元素原子的最外层电子数比次外层电子数少2,且是短周期元素,所以是S元素,则D是Na元素;A、B、D、E这四种元素,每一种与C元素都能形成原子个数比不相同的若干种化合物,所以C是O元素,
(1)同一主族元素,元素的非金属性随着原子序数的增大而减小,所以得电子能力减弱,C和E两种元素相比较,原子得电子能力较强的元素为C即O元素,氧为第二周期 VIA族;
a.元素原子得电子能力强弱,与单质的沸点无关,故a错误;
b.两种元素形成化合物时非金属性强的显负价,则二者形成的化合物中,C元素的原子显负价,说明C的得电子能力强,故b正确;
c.元素的氢化物越稳定,元素的非金属性越强,其原子的得电子能力越强,故c正确;
故答案为:第二周期 VIA族;bc;
(2)氨气和硝酸反应生成硝酸铵,硝酸铵中含有离子键、共价键,则盐M中含有的化学键类型有离子键、共价键;
故答案为:离子键、共价键;
(3)A、B、C、E可形成两种酸式盐(均含有该四种元素),形成的酸式盐一个是硫酸氢盐,一个是亚硫酸氢盐,其离子方程式为HSO3-+H+=H2O+SO2↑;
故答案为:HSO3-+H+=H2O+SO2↑;
(4)B2A4是一种可燃性液体,B2A4是N2H4,燃料电池中,负极上燃料失电子发生氧化反应,正极上氧化剂得电子被还原,所以负极上的电极反应式为N2H4+4OH--4e-=4H2O+N2;
故答案为:N2H4+4OH--4e-=4H2O+N2;
(5)已知1molD与水反应放出283.5kJ的热量,则钠和水反应生成氢氧化钠和氢气,1molD与水反应放出283.5kJ的热量,则2mol钠和水反应放出567KJ能量,
故答案为:2Na(s)+2H2O(l)=2NaOH(aq)+H2(g)△H=-567kJ/mol.
(1)同一主族元素,元素的非金属性随着原子序数的增大而减小,所以得电子能力减弱,C和E两种元素相比较,原子得电子能力较强的元素为C即O元素,氧为第二周期 VIA族;
a.元素原子得电子能力强弱,与单质的沸点无关,故a错误;
b.两种元素形成化合物时非金属性强的显负价,则二者形成的化合物中,C元素的原子显负价,说明C的得电子能力强,故b正确;
c.元素的氢化物越稳定,元素的非金属性越强,其原子的得电子能力越强,故c正确;
故答案为:第二周期 VIA族;bc;
(2)氨气和硝酸反应生成硝酸铵,硝酸铵中含有离子键、共价键,则盐M中含有的化学键类型有离子键、共价键;
故答案为:离子键、共价键;
(3)A、B、C、E可形成两种酸式盐(均含有该四种元素),形成的酸式盐一个是硫酸氢盐,一个是亚硫酸氢盐,其离子方程式为HSO3-+H+=H2O+SO2↑;
故答案为:HSO3-+H+=H2O+SO2↑;
(4)B2A4是一种可燃性液体,B2A4是N2H4,燃料电池中,负极上燃料失电子发生氧化反应,正极上氧化剂得电子被还原,所以负极上的电极反应式为N2H4+4OH--4e-=4H2O+N2;
故答案为:N2H4+4OH--4e-=4H2O+N2;
(5)已知1molD与水反应放出283.5kJ的热量,则钠和水反应生成氢氧化钠和氢气,1molD与水反应放出283.5kJ的热量,则2mol钠和水反应放出567KJ能量,
故答案为:2Na(s)+2H2O(l)=2NaOH(aq)+H2(g)△H=-567kJ/mol.
点评:本题综合性较大,涉及结构性质越位置关系、元素周期律、化学键、离子方程式,原电池原理的应用、热化学方程式的书写等,题目难度中等,是物质结构的综合性题目,是对学生综合能力的考查,根据原子结构和元素在周期表中的位置推断出元素是解题的关键.

练习册系列答案
相关题目
下列关于胶体的叙述不正确的是( )
| A、红色激光束能透过小烧杯中的氢氧化铁胶体,但不能透过小烧杯中较浓的硫酸铜溶液 |
| B、胶体的丁达尔效应是胶体粒子对可见光散射而形成的 |
| C、胶体化学是随20世纪未纳米科技兴起而产生的 |
| D、纳米粒子的大小与胶体粒子相当,但纳米粒子的体系不一定是胶体 |
用惰性电极电解下列各稀溶液,经一段时间后,溶液的pH保持不变的是( )
| A、CuCl2 |
| B、NaCl溶液 |
| C、H2SO4溶液 |
| D、K2SO4溶液 |
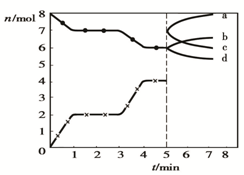 炼铁的还原剂CO是由焦炭和CO2反应而得,现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO2(g)?2CO(g)△H=Q kJ/mol.如图为CO2、CO的物质的量n随时间t的变化关系图,下列说法正确的是( )
炼铁的还原剂CO是由焦炭和CO2反应而得,现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO2(g)?2CO(g)△H=Q kJ/mol.如图为CO2、CO的物质的量n随时间t的变化关系图,下列说法正确的是( )| A、0~1min,v(CO)=1mol/(L?min);1~3min时,v(CO)=v(CO2) | ||||
B、当容器内的压强不变时,反应一定达到平衡状态,且
| ||||
C、3min时温度由T1升高到T2,则Q>0,重新平衡时
| ||||
| D、5min时再充入一定量的CO,a、b分别曲线表示n(CO)、n(CO2)的变化 |
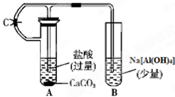 根据如图所示装置,请回答:
根据如图所示装置,请回答: