题目内容
环境保护和能源开发是当今社会的热门话题.根据所学化学知识解答下列问题:
(1)在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染.
已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol;
2C(s)+O2(g)=2CO(g)△H=-221.0kJ/mol;
C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol
尾气转化的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g)△H= .
请在答题纸中画出这个反应在反应过程中体系能量变化示意图,并进行必要标注:
(2)汽车尾气分析仪对CO的分析是以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.

下列说法错误的是 .
A.负极的电极反应式为:CO+O2--2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
(3)某新型铝-空气燃料电池,以铝为负极,在正极通入空气,若以NaCl溶液或NaOH溶液为电解质溶液,放电时正极反应都为O2+2H2O+4e-=4OH-.那么若以NaOH溶液为电解质溶液,电池负极反应为: ;若以NaCl溶液为电解质溶液,则总反应为: .
(1)在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染.
已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol;
2C(s)+O2(g)=2CO(g)△H=-221.0kJ/mol;
C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol
尾气转化的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=
请在答题纸中画出这个反应在反应过程中体系能量变化示意图,并进行必要标注:
(2)汽车尾气分析仪对CO的分析是以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.

下列说法错误的是
A.负极的电极反应式为:CO+O2--2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
(3)某新型铝-空气燃料电池,以铝为负极,在正极通入空气,若以NaCl溶液或NaOH溶液为电解质溶液,放电时正极反应都为O2+2H2O+4e-=4OH-.那么若以NaOH溶液为电解质溶液,电池负极反应为:
考点:用盖斯定律进行有关反应热的计算,化学电源新型电池,电解原理
专题:电化学专题
分析:(1)根据盖斯定律把已知方程式加减得出NO与CO催化转化成N2和CO2的化学方程式,焓变相应的加减,从而得出其热化学反应方程式;该反应为放热反应,反应物的能量大于生成物的能量;
(2)该装置是原电池,负极上一氧化碳失电子发生氧化反应,正极上氧气得电子发生还原反应,原电池放电时电子从负极流向正极,阴离子向负极移动,一氧化碳的含量越大,原电池放电时产生的电流越大;
(3)碱性条件下,Al在负极失电子生成AlO2-;以NaCl溶液为电解质溶液时Al与氧气、水反应生成氢氧化铝.
(2)该装置是原电池,负极上一氧化碳失电子发生氧化反应,正极上氧气得电子发生还原反应,原电池放电时电子从负极流向正极,阴离子向负极移动,一氧化碳的含量越大,原电池放电时产生的电流越大;
(3)碱性条件下,Al在负极失电子生成AlO2-;以NaCl溶液为电解质溶液时Al与氧气、水反应生成氢氧化铝.
解答:
解:(1)N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol①
2C(s)+O2(g)=2CO(g)△H=-221.0kJ/mol②
C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol ③
由盖斯定律得③×2-②-①,则NO (g)+2CO(g)=N2(g)+2CO2(g)所以△H=(-393.5kJ/mol)×2-(-221.0kJ/mol)-(+180.5kJ/mol)=-746.5 kJ/mol,
该反应为放热反应,反应物的能量大于生成物的能量,则该反应在反应过程中体系能量变化示意图为: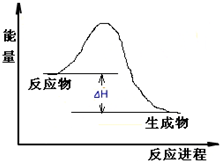 ;
;
故答案为:-746.5 kJ/mol; ;
;
(2)A.该装置是原电池,通入一氧化碳的电极a是负极,负极上一氧化碳失电子发生氧化反应,电极反应式为:CO+O2--2e-═CO2,故A正确;
B.工作时电极b作正极,O2-由电极b流向电极a,故B错误;
C.该装置是原电池,通入一氧化碳的电极a是负极,通入空气的电极是正极,原电池放电时,电子从负极a通过传感器流向电极b,故C正确;
D.一氧化碳的含量越大,CO失去的电子的物质的量越大,原电池放电时产生的电流越大,故D正确;
故答案为:B;
(3)碱性条件下,Al在负极失电子生成AlO2-,则负极的电极反应为:Al+4OH--3e-=AlO2-+2H2O;以NaCl溶液为电解质溶液时Al与氧气、水反应生成氢氧化铝,则电池的总反应为4Al+3O2+6H2O=4Al(OH)3,
故答案为:Al+4OH--3e-=AlO2-+2H2O;4Al+3O2+6H2O=4Al(OH)3.
2C(s)+O2(g)=2CO(g)△H=-221.0kJ/mol②
C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol ③
由盖斯定律得③×2-②-①,则NO (g)+2CO(g)=N2(g)+2CO2(g)所以△H=(-393.5kJ/mol)×2-(-221.0kJ/mol)-(+180.5kJ/mol)=-746.5 kJ/mol,
该反应为放热反应,反应物的能量大于生成物的能量,则该反应在反应过程中体系能量变化示意图为:
 ;
;故答案为:-746.5 kJ/mol;
 ;
; (2)A.该装置是原电池,通入一氧化碳的电极a是负极,负极上一氧化碳失电子发生氧化反应,电极反应式为:CO+O2--2e-═CO2,故A正确;
B.工作时电极b作正极,O2-由电极b流向电极a,故B错误;
C.该装置是原电池,通入一氧化碳的电极a是负极,通入空气的电极是正极,原电池放电时,电子从负极a通过传感器流向电极b,故C正确;
D.一氧化碳的含量越大,CO失去的电子的物质的量越大,原电池放电时产生的电流越大,故D正确;
故答案为:B;
(3)碱性条件下,Al在负极失电子生成AlO2-,则负极的电极反应为:Al+4OH--3e-=AlO2-+2H2O;以NaCl溶液为电解质溶液时Al与氧气、水反应生成氢氧化铝,则电池的总反应为4Al+3O2+6H2O=4Al(OH)3,
故答案为:Al+4OH--3e-=AlO2-+2H2O;4Al+3O2+6H2O=4Al(OH)3.
点评:本题考查了盖斯定律的应用、化学反应中的能量变化、原电池原理等,注意把握原电池中电极方程式的书写方法及溶液的酸碱性对反应的影响,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
分类法是一种行之有效、简单易行的科学方法.下列关于K2CO3的分类不正确的是( )
| A、钾盐 | B、有机物 |
| C、化合物 | D、碳酸盐 |
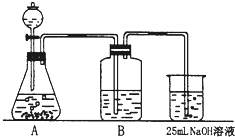 Na2CO3是一种很重要的化学物质,某学生拟在实验室中制备.下面是他的实验过程.用50mL NaOH溶液吸收CO2气体制备Na2CO3.为了防止通入的CO2过量而生成NaHCO3,他设计了如下步骤:
Na2CO3是一种很重要的化学物质,某学生拟在实验室中制备.下面是他的实验过程.用50mL NaOH溶液吸收CO2气体制备Na2CO3.为了防止通入的CO2过量而生成NaHCO3,他设计了如下步骤: 乙醇是生活中常见的一种有机物,它的分子结构模型如图所示:
乙醇是生活中常见的一种有机物,它的分子结构模型如图所示: