题目内容
13.等物质的量的下列有机物,在相同条件下完全燃烧,耗氧量最多的是( )| A. | C5H6 | B. | C4H6 | C. | C4H8O | D. | C5H6O2 |
分析 等物质的量均设为1mol,有机物CxHyOz完全燃烧耗氧量取决于(x+$\frac{y}{4}$-$\frac{z}{2}$),(x+$\frac{y}{4}$-$\frac{z}{2}$)的值越大,则其耗氧量越大,以此来解答.
解答 解:设有机物均为1mol,则
A.1molC5H6消耗氧气为:1mol×(5+$\frac{6}{4}$)=6.5mol;
B.1molC4H6消耗氧气为:1mol×(4+$\frac{6}{4}$)=5.5mol;
C.1molC4H8O消耗氧气为:1mol×(4+$\frac{8}{4}$-$\frac{1}{2}$)=5.5mol;
D.1molC5H6O2消耗氧气为:1mol×(5+$\frac{6}{4}$-$\frac{2}{2}$)=5.5mol,
根据分析可知,物质的量相等时耗氧量最大的为A,
故选A.
点评 本题考查有机物燃烧反应的计算,为高频考点,把握燃烧规律及消耗氧气的计算方法为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
14.不饱和内酯是各种杀菌剂、杀虫剂、高分子改性剂、医药品的原料或中间体,合成不饱和内酯已引起人们极大的兴趣.以下是利用CO2合成一种不饱和内酯的反应方程式:2Me-C≡C-Me+CO2$\stackrel{适当条件}{→}$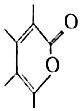 以下说法正确的是( )
以下说法正确的是( )
 以下说法正确的是( )
以下说法正确的是( )| A. | 一Me基团的电子式为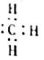 | |
| B. | 该合成过程的反应类型属于加成反应 | |
| C. | 产物与 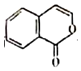 互为同分异构体 互为同分异构体 | |
| D. | 产物可与H2发生加成反应,反应的物质的量之比为1:3 |
15.短周期元素a、b、c、d分属三个周期,且原子序数依次增大.其中b与a、c两种元素均可形成原子个数比为1:1或1:2的化合物,a、c的原子具有相同的最外层电子数,b、d形成的一种化合物在工业上是一种新型自来水消毒剂.下列说法一定正确的是( )
| A. | d的含氧酸是强酸 | |
| B. | 离子半径:d>c>b | |
| C. | b、c、d形成的化合物中只含离子键 | |
| D. | a、c形成的离子化合物具有还原性,可与水反应 |
1.工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]的工艺流程如下:
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
回答下列问题:
(1)反应I溶液中存在的金属阳离子有Fe2+、Al3+.
(2)加入NaHCO3的目的是调节pH,使溶液中的Al3+(填“Fe3+”、“Fe2+”或“A13+”)沉淀.该工艺流程中“搅拌”的作用是加快反应速率.
(3)反应II的离子方程式为2H++Fe2++NO2-=Fe3++NO↑+H2O.在实际生产中,反应II常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作为氧化剂.若参与反应的O2有11.2L(标准状况),则相当于节约NaNO2物质的量为2mol.
(4)碱式硫酸铁溶于水后产生的[Fe(OH)]2+离子,可部分水解生成${[{F{e_2}{{({OH})}_4}}]^{2+}}$聚合离子.该水解反应的离子方程式为2Fe(OH)2++2H2O?Fe2(OH)42++2H+.
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)反应I溶液中存在的金属阳离子有Fe2+、Al3+.
(2)加入NaHCO3的目的是调节pH,使溶液中的Al3+(填“Fe3+”、“Fe2+”或“A13+”)沉淀.该工艺流程中“搅拌”的作用是加快反应速率.
(3)反应II的离子方程式为2H++Fe2++NO2-=Fe3++NO↑+H2O.在实际生产中,反应II常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作为氧化剂.若参与反应的O2有11.2L(标准状况),则相当于节约NaNO2物质的量为2mol.
(4)碱式硫酸铁溶于水后产生的[Fe(OH)]2+离子,可部分水解生成${[{F{e_2}{{({OH})}_4}}]^{2+}}$聚合离子.该水解反应的离子方程式为2Fe(OH)2++2H2O?Fe2(OH)42++2H+.
18.蓄电池是一种可以反复充电、放电的装置,有一种蓄电池在充电(电解池)和放电(原电池)时发生的反应是NiO2+Fe+2H2O$?_{充电}^{放电}$ Fe(OH)2+Ni(OH)2,用该蓄电池电解(阴、阳极均为惰性电极)M(NO3)x溶液时,若此蓄电池工作一段时间后消耗0.36g 水.电解M(NO3)x溶液时某一极质量增加m g,金属M的相对原子质量(用m、x表示)的计算式为( )
| A. | 20mx | B. | 20x/m | C. | 25mx | D. | 50m/x |
5.对于化学反应方向的确定,下列说法正确的是( )
| A. | 在温度、压强一定的条件下,仅熵因素决定一个化学反应的方向 | |
| B. | 温度、压强一定时,放热的熵增加反应一定能自发进行 | |
| C. | 反应焓变是决定反应能否自发进行的唯一因素 | |
| D. | 固体的溶解过程与熵变无关 |
2.下列有关工业生产的叙述中正确的是( )
| A. | 硫酸工业中,为了提高SO2的转化率,使用五氧化二钒作催化剂 | |
| B. | 合成氨中通过及时分离液态氨来提高化学反应速率 | |
| C. | 电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小 | |
| D. | 电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的C12进入阳极室 |
3.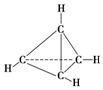 一种有机物的化学式为C4H4,分子结构如图所示,将该有机物与适量氯气混合后光照,生成的氯代烃的种类共有( )
一种有机物的化学式为C4H4,分子结构如图所示,将该有机物与适量氯气混合后光照,生成的氯代烃的种类共有( )
 一种有机物的化学式为C4H4,分子结构如图所示,将该有机物与适量氯气混合后光照,生成的氯代烃的种类共有( )
一种有机物的化学式为C4H4,分子结构如图所示,将该有机物与适量氯气混合后光照,生成的氯代烃的种类共有( )| A. | 1种 | B. | 2种 | C. | 4种 | D. | 6种 |