题目内容
关于物质的分类正确的是( )
| A、SO2、CO2、CO、NO2都是酸性氧化物 |
| B、Na2O、Na2O2、Fe2O3、CuO都是碱性氧化物 |
| C、HCl、HClO、HNO3、HClO4都是强酸 |
| D、NaOH、KOH、Ba(OH)2、Ca(OH)2都是强碱 |
考点:酸、碱、盐、氧化物的概念及其相互联系
专题:
分析:A、能和碱反应生成盐和水的氧化物属于酸性氧化物;
B、碱性氧化物是指能跟酸起反应,生成盐和水的氧化物;
C、强酸是强电解质,H+能完全电离;
D、强碱是强电解质,OH-能完全电离;
B、碱性氧化物是指能跟酸起反应,生成盐和水的氧化物;
C、强酸是强电解质,H+能完全电离;
D、强碱是强电解质,OH-能完全电离;
解答:
解:A、SO2、CO2是酸性氧化物,但CO既不能与酸反应生成盐和水,也不能和碱反应生成盐和水,故是不成盐氧化物;NO2与碱反应生成盐和水的同时,还生成NO,故不是酸性氧化物,故A错误;
B、Na2O2与酸反应除了生成盐和水还生成氧气,故不是碱性氧化物,故B错误;
C、HClO是弱酸,故C错误;
D、NaOH、KOH、Ba(OH)2、Ca(OH)2都是强碱,故D正确.
故选D.
B、Na2O2与酸反应除了生成盐和水还生成氧气,故不是碱性氧化物,故B错误;
C、HClO是弱酸,故C错误;
D、NaOH、KOH、Ba(OH)2、Ca(OH)2都是强碱,故D正确.
故选D.
点评:本题考查了酸性氧化物、碱性氧化物和酸性、碱性强弱的判断,根据定义来判断,属于基础性题目.

练习册系列答案
相关题目
下列有关元素的性质及其递变规律正确的是( )
| A、同周期金属元素的最外层电子越多,其原子失电子能力越强 |
| B、对于HF、HCl、HBr其熔、沸点随其相对分子质量的增大而升高 |
| C、ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 |
| D、同主族元素的简单阴离子还原性越强,其盐类的水解程度越大 |
咖喱是一种烹饪辅料,若白衬衣被咖喱汁玷污后,用普通的肥皂洗涤时,会发现黄色污渍变为红色,经水漂洗后红色又变黄色.据此现象,你认为咖喱汁与下列何种试剂可能有相似的化学作用( )
| A、品红溶液 | B、石蕊溶液 |
| C、氯水 | D、碘化钾-淀粉溶液 |
 氮化硅是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
氮化硅是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得: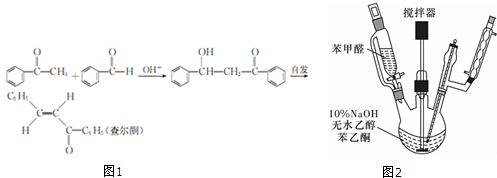
 试回答:
试回答: