题目内容
钠与水反应时,观察到的现象是( )
①钠浮在水面上
②钠先沉入水中
③钠熔成光亮的小球
④四处游动
⑤发出“嘶嘶”的响声,甚至发生轻微的爆炸
⑥滴入酚酞溶液变红.
①钠浮在水面上
②钠先沉入水中
③钠熔成光亮的小球
④四处游动
⑤发出“嘶嘶”的响声,甚至发生轻微的爆炸
⑥滴入酚酞溶液变红.
| A、全部 | B、①③④⑤⑥ |
| C、②③⑥ | D、②③④⑤⑥ |
考点:钠的化学性质
专题:金属概论与碱元素
分析:钠与水反应时产生的各种现象如下:钠浮在水面,然后熔化成闪亮黄色小球,在水面游动并发出嘶嘶的响声,溶液由无色变为红色.原因如下:浮:密度比水小,熔:熔点低,游 嘶:剧烈反应,红:生成碱性物质.
解答:
解:①钠浮在水面上,密度比水小,故正确;
②钠先沉入水中,密度比水小,应浮在水面上,故错误;
③钠熔成光亮的小球,熔点低,故正确;
④四处游动,因为反应剧烈,故正确;
⑤发出“嘶嘶”的响声,甚至发生轻微的爆炸,因为反应剧烈,故正确;
⑥滴入酚酞溶液变红,因为生成氢氧化钠成碱性,故正确;
故选:B.
②钠先沉入水中,密度比水小,应浮在水面上,故错误;
③钠熔成光亮的小球,熔点低,故正确;
④四处游动,因为反应剧烈,故正确;
⑤发出“嘶嘶”的响声,甚至发生轻微的爆炸,因为反应剧烈,故正确;
⑥滴入酚酞溶液变红,因为生成氢氧化钠成碱性,故正确;
故选:B.
点评:本题考查了钠与水的反应.应从钠的强还原性和钠的物理性质来理解钠与水反应的现象.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
自然界里常见金属元素存在最多的是铝,其次是铁,铜的含量较少.然而人类冶炼金属获得成功最早的反而是含量少的铜,含量最多的铝最迟冶炼出来,究其原因,合理的是( )
| A、铜矿较易还原,铝矿很难还原 |
| B、铜矿颜色较深,易发现;铝矿颜色较浅,不易发现 |
| C、矿石在地下埋藏,铜矿最浅,容易开发,铝矿埋得深,难开发 |
| D、以上说法都是错误的 |
某反应2AB(g)?C(g)+3D(g)只有在高温时才能自发进行,则该反应的△H、△S应为( )
| A、△H<0,△S>0 |
| B、△H<0,△S<0 |
| C、△H>0,△S>0 |
| D、△H>0,△S<0 |
下列说法不正确的是( )
| A、将标准状况下11.2L HCl溶于水,配成250mL盐酸,溶液的物质的量浓度为2mol/L |
| B、硫酸和磷酸的摩尔质量相等 |
| C、同温同压下,相同质量的二氧化碳和二氧化硫的体积比是16:11 |
| D、2.24L CO和CO2混合气体中含有的碳原子数目为0.1NA |
下列说法正确的是( )
| A、若苛性钠放在纸上称量,会使所配制的苛性钠溶液浓度偏大 |
| B、可以用向下排空气法收集氢气、氨气、一氧化碳等气体 |
| C、电解质溶液导电,肯定发生了化学变化 |
| D、某些取出的化学试剂,未用完的可以放回愿试剂瓶,如:K、Na2CO3 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、甲基橙呈红色的溶液中:MnO4-、Al3+、C2H5OH、SO42- |
| B、常温下的溶液:KW/c(H+)=0.1mol/L的溶液:K+、Na+、SiO32-、NO3- |
| C、稀硫酸中:K+、Mg2+、AlO2-、S2O32- |
| D、加入苯酚显紫色的溶液:K+、NH4+、Cl-、I- |
下列现象或应用不能用胶体的知识解释的是( )
| A、肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 |
| B、氯化钙溶液中加入碳酸钠溶液会出现白色沉淀 |
| C、水泥、冶金工厂常用高压电除去工厂烟尘,减少对空气的污染 |
| D、土壤表面积巨大且一般带负电,能吸收NH4+等营养离子,使土壤具有保肥能力 |
下列各项叙述正确的是( )
| A、清晨,在树林中,常看到从枝叶间透过的一道道光柱,这是胶体产生的丁达尔效应 |
| B、某固体A能导电,一定是金属 |
| C、由同种元素组成的物质肯定属于纯净物 |
| D、由氯化铵溶液呈弱酸性可知氯化铵是弱电解质 |
如图所示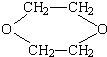 是一种常见的溶剂,是它可以通过下列路线制得:
是一种常见的溶剂,是它可以通过下列路线制得:
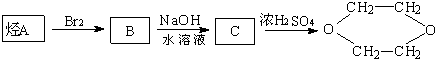
则A可能是( )
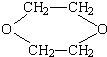 是一种常见的溶剂,是它可以通过下列路线制得:
是一种常见的溶剂,是它可以通过下列路线制得:
则A可能是( )
| A、乙烯 | B、乙醇 | C、乙二醇 | D、乙醚 |