题目内容
14. 钒及其化合物非常丰富.钒可用于生产合金钢、航天用的钒钛合金及化工催化剂等.
钒及其化合物非常丰富.钒可用于生产合金钢、航天用的钒钛合金及化工催化剂等.(1)V基态核外电子排布式为[Ar]3d34s2或1s22s22p63s23p63d34s2.
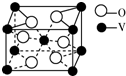
(2)某钒的氧化物的晶胞如图所示,则该氧化物的化学式为VO2.
(3)利用NH4VO3制备催化剂V2O5的反应如下:2NH4VO3$\frac{\underline{\;\;△\;\;}}{\;}$V2O5+2NH3↑+H2O.与NH3互为等电子体的一种阳离子为H3O+(填化学式).
(4)常温下V(CO)6为蓝绿色固体,易挥发,易升华,不溶于水,溶于乙醚、吡啶(N).
①固态V(CO)6属于分子 晶体.
②N分子中N原子的杂化类型为sp2.
③V(CO)6中含有的化学键有ABC(填字母).
A.σ键 B.π键 C.配位键 D.非极性键.
分析 (1)V的核电荷数为23,其基态核外电子排布式为[Ar]3d34s2或1s22s22p63s23p63d34s2;
(2)用均摊法晶胞中钒8×$\frac{1}{8}$+1=2,而氧的原子个数为4×$\frac{1}{2}$+2=4;
(3)与NH3互为等电子体的一种阳离子为水合氢离子;
(4)常温下V(CO)6为蓝绿色固体,易挥发,易升华,不溶于水,溶于乙醚、吡啶(N).
①易挥发,易升华,固态V(CO)6属于分子晶体;
②吡啶(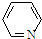 ),分子中N原子的杂化类型为sp2;
),分子中N原子的杂化类型为sp2;
③V(CO)6中含有的化学键有σ键、π键、配位键.
解答 解:(1)V的核电荷数为23,其基态核外电子排布式为[Ar]3d34s2或1s22s22p63s23p63d34s2,故答案为:[Ar]3d34s2或1s22s22p63s23p63d34s2;
(2)用均摊法晶胞中钒8×$\frac{1}{8}$+1=2,而氧的原子个数为4×$\frac{1}{2}$+2=4,所以则该氧化物的化学式为VO2,故答案为:VO2;
(3)与NH3互为等电子体的一种阳离子为水合氢离子,故答案为:H3O+;
(4)①易挥发,易升华,固态V(CO)6属于分子晶体;
②吡啶(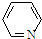 ),分子中N原子的杂化类型为sp2;
),分子中N原子的杂化类型为sp2;
③V(CO)6中含有的化学键有σ键、π键、配位键,故答案为:①分子;②sp2;③ABC.
点评 本题考查较为综合,涉及电子排布、化学键、杂化、晶体类型等多个方面的知识,注意电子排布式的书写方法,侧重物质结构与性质的考查,题目难度较大.

练习册系列答案
相关题目
2.常温下,反应2H2S(g)+SO2(g)═3S(s)+2H2O(l)能自发进行.下列说法正确的是( )
| A. | 该反应为吸热反应 | |
| B. | 该反应中,SO2为还原剂 | |
| C. | 1 mol H2S中含有的共价键的数目为3 mol | |
| D. | 常温下,H2S的还原性强于S的还原性 |
9.下列说法正确的是( )
| A. | 若电解熔融MgCl2产生1 mol Mg,理论上转移的电子数约为2×6.02×1023 | |
| B. | 海轮船体镶嵌锌块是牺牲阳极的阴极保护法,防止船体被腐蚀 | |
| C. | 室温下,pH均为3的盐酸和NH4Cl溶液中,水的电离程度相同 | |
| D. | 一定条件下反应2SO2+O2?2SO3达到平衡时,v正(O2)=2v逆(SO3) |
3.己知反应2H2(g)+02(g)=2H20(1)△H=-285.8kJ•mo1-1,下列正确的是( )
| A. | E(反应物)>E(生成物) | B. | E(反应物)<E(生成物) | C. | 反应放热 | D. | 反应吸热 |




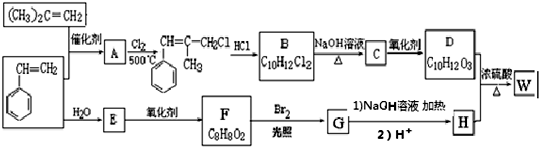
 .
.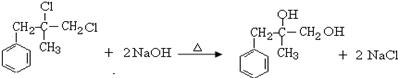 ;由D生成高分子化合物的方程式为
;由D生成高分子化合物的方程式为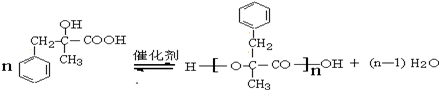 .
.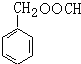 (写结构简式).
(写结构简式).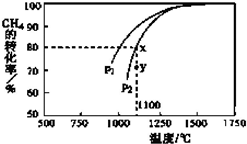 能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.
能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.