题目内容
13.铝在人体中积累可使人慢性中毒,世界卫生组织将铝确定为食品污染源之一而加以控制.铝在下列使用场合中,不必要加以控制的是( )| A. | 制造炊具 | B. | 制儿童玩具油漆 | C. | 制牙膏皮 | D. | 炼铝厂制造铝锭 |
分析 铝在人体内积累可使人慢性中毒,铝进入人体的主要途径是通过消化系统,既然铝是食品污染源之一,凡与人的食用物品及口腔接触的物品都必须控制铝的使用,据此分析解答.
解答 解:A.用铝制作炊具时,会使铝进入人体,需要加以控制,故A不选;
B.制儿童玩具油漆,铝与人直接接触,与人体健康有关,需控制,故B不选;
C.牙膏皮上的铝能随通过消化系统进入人体,需要加以控制,故C不选;
D.炼铝厂制造铝锭与人体健康无关,无需控制,故D选;
故选D.
点评 本题考查铝的性质与人体健康,掌握铝可能进入人体的途径(如铝可以通过饮食、药物等途径进入人体从而危害人体健康)是解题的关键,题目难度不大.

练习册系列答案
相关题目
19.下列陈述I、II均正确且有因果关系的是( )
| 选项 | 陈述I | 陈述II |
| A | Na2O2具有漂白性 | Na2O2可用于潜水呼吸用氧 |
| B | SiO2有导电性 | SiO2可用于制作光导纤维 |
| C | 浓H2SO4有脱水性 | 浓H2SO4可用于干燥Cl2、SO2 |
| D | CO有还原性 | CO可用来冶炼生铁 |
| A. | A | B. | B | C. | C | D. | D |
4.科学家在利用无土栽培培养一些名贵花卉时,培养液中添加了多种必需元素,其配方如下,其中植物根吸收最少的离子是( )
| 离子 | K+ | Mg2+ | Ca2+ | NO3- | H2PO4- | SO42- | Zn2+ |
| $\frac{培养液浓度}{nmol•{L}^{-1}}$ | 1 | 0.25 | 1 | 2 | 1 | 0.25 | 1 |
| A. | Zn2+ | B. | SO42- | C. | Ca2+ | D. | H2PO4- |
1.已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中的信息,回答下列问题:
(1)表中硫酸的质量分数为$\frac{98{c}_{1}}{1000{ρ}_{1}}$(不写单位,用含c1、ρ1的代数式表示).
(2)物质的量浓度为c1mol•L-1的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为0.5c1mol•L-1.
(3)物质的量浓度为c2mol•L-1的氨水与$\frac{1}{5}$c2mol•L-1的氨水等质量混合,所得溶液的密度大于(填“大于”、“小于”或“等于”,下同) ρ2g•cm-3,所得溶液的物质的量浓度大于$\frac{3}{5}$c2mol•L-1(设混合后溶液的体积变化忽略不计)
(4)若将稀硫酸与氨水混合,写出其反应的离子方程式NH3•H2O+H+=NH4++H2O.
| 溶质的物质的量浓度/mol•L-1 | 溶液的密度/g•cm-3 | 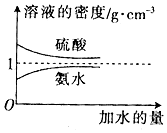 | |
| 硫酸 | c1 | ρ1 | |
| 氨水 | c2 | ρ2 |
(2)物质的量浓度为c1mol•L-1的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为0.5c1mol•L-1.
(3)物质的量浓度为c2mol•L-1的氨水与$\frac{1}{5}$c2mol•L-1的氨水等质量混合,所得溶液的密度大于(填“大于”、“小于”或“等于”,下同) ρ2g•cm-3,所得溶液的物质的量浓度大于$\frac{3}{5}$c2mol•L-1(设混合后溶液的体积变化忽略不计)
(4)若将稀硫酸与氨水混合,写出其反应的离子方程式NH3•H2O+H+=NH4++H2O.
5.下列有关气体体积的叙述中,正确的是( )
| A. | 一定温度和压强下,各种气体物质体积的大小由构成气体的分子大小决定 | |
| B. | 一定温度和压强下,各种气态物质体积的大小,由构成气体的原子数决定 | |
| C. | 无论外界条件是否相同,不同的气体,若物质的量不同,则它们所含的分子数也不同 | |
| D. | 相同状况下,相同微粒数的Fe、H2O、H2的体积相同 |
2.下列每组中的两种物质间不互为同分异构体的是( )
| A. | CH3CH2CH2CH3与CH3CH(CH3)2 | B. | CH3CH═C(CH3)2与CH2═CHCH(CH3)2 | ||
| C. | 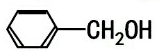 与 与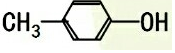 | D. | 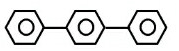 与 与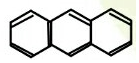 |