题目内容
下列制取单质的反应中,化合物作还原剂的是( )
| A、Zn+H2SO4═ZnSO4+H2↑ |
| B、C+2CuO═2Cu+CO2 |
| C、Br2+2NaI═2NaBr+I2 |
| D、Cu+2AgNO3═2Ag+Cu(NO3)2 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:化合物作还原剂,则化合物中某元素的化合价升高,以此来解答.
解答:
解:A.硫酸中H元素的化合价降低,化合物为氧化剂,故A不选;
B.氧化铜中Cu元素的化合价降低,化合物为氧化剂,故B不选;
C.碘化钠中I元素的化合价升高,化合物为还原剂,故C选;
D.硝酸银中Ag元素的化合价降低,化合物为氧化剂,故D不选;
故选:C.
B.氧化铜中Cu元素的化合价降低,化合物为氧化剂,故B不选;
C.碘化钠中I元素的化合价升高,化合物为还原剂,故C选;
D.硝酸银中Ag元素的化合价降低,化合物为氧化剂,故D不选;
故选:C.
点评:本题考查氧化还原反应,侧重还原剂判断的考查,为高考常见题型,把握反应中元素的化合价变化为解答的关键,题目难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
下列反应的离子方程式不正确的是( )
| A、向碳酸氢钙溶液中加入过量氢氧化钠:Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- |
| B、等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+NH4++HCO3-═BaCO3↓+NH3?H2O+H2O |
| C、在溴化亚铁溶液中通入过量的氯气:Cl2+2Fe2++2Br-═2Fe3++2Cl-+Br2 |
| D、过量CO2通入氢氧化钠溶液中:CO2+OH-═HCO3- |
亚硝酸(HNO2)既可以做氧化剂又可作还原剂,当它在反应中作氧化剂时,可能生成的物质是( )
| A、N2 |
| B、N2O3 |
| C、HNO3 |
| D、NO2 |
设NA代表阿佛加德罗常数,下列说法正确的是( )
| A、62 g Na2O与78gNa2O2中所含阴离子的个数比为1:2 |
| B、质量相等的两份气体,一份是SO2,另一份是SO3,这两份气体中,SO2与SO3所含氧原子个数之比是6:5 |
| C、在标准状况下,0.5NA个水分子所占体积是11.2 L |
| D、500 mL 1 mol/L Fe2(SO4)3溶液,同250 mL 3 mol/L的Na2SO4溶液所含硫酸根离子的物质的量浓度之比为1:1 |
常温下,下列溶液中一定能大量共存的离子组是( )
| A、能使甲基橙变红的溶液:NH4+、Na+、SO42-、Fe3+ |
| B、无色澄清溶液:K+、HCO3-、SO42-、Al3+ |
| C、与金属铝反应能放出氢气的溶液:NH4+、NO3-、SO42-、Na+ |
| D、水电离产生的c(H+)=1×10-12mol/L的溶液:HCO3-、NH4+、Cl-、Ca2+ |
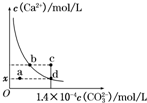 室温时,CaCO3在水中的溶解平衡曲线如图所示,已知:25℃其溶度积为2.8×10-9 mol2/L2,下列说法不正确的是( )
室温时,CaCO3在水中的溶解平衡曲线如图所示,已知:25℃其溶度积为2.8×10-9 mol2/L2,下列说法不正确的是( )| A、x数值为2×10-5 |
| B、c点时有碳酸钙沉淀生成 |
| C、加入蒸馏水可使溶液由d点变到a点 |
| D、b点与d点对应的溶度积相等 |

 甲醇是一种可再生能源,具有广泛的开发和应用前景.
甲醇是一种可再生能源,具有广泛的开发和应用前景. 将35.8gNa2CO3和NaHCO3的固体混合物溶于足量水中,向其中逐滴加入1mol?L-1的盐酸至不再产生气体为止,测得共产生CO28.96L(标准状况)(气体溶解忽略不计).回答:
将35.8gNa2CO3和NaHCO3的固体混合物溶于足量水中,向其中逐滴加入1mol?L-1的盐酸至不再产生气体为止,测得共产生CO28.96L(标准状况)(气体溶解忽略不计).回答: