题目内容
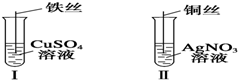 按如图所示操作,充分反应后:
按如图所示操作,充分反应后:(1)Ⅰ中发生反应的离子方程式为
(2)Ⅱ中铜丝上观察到的现象是
(3)结合Ⅰ、Ⅱ实验现象可知,Fe、Cu、Ag的还原性顺序为
考点:常见金属元素的单质及其化合物的综合应用,常见金属的活动性顺序及其应用
专题:
分析:(1)I中发生Fe与硫酸铜的反应,生成硫酸亚铁和Cu;
(2)Ⅱ中发生Cu与硝酸银的反应,生成硝酸铜和Ag;
(3)由反应及元素的化合价变化可知,还原性的还原性大于还原产物的还原性.
(2)Ⅱ中发生Cu与硝酸银的反应,生成硝酸铜和Ag;
(3)由反应及元素的化合价变化可知,还原性的还原性大于还原产物的还原性.
解答:
解:(1)I中发生Fe与硫酸铜的反应,生成硫酸亚铁和Cu,离子反应为Fe+Cu2+═Fe2++Cu,故答案为:Fe+Cu2+═Fe2++Cu;
(2)Ⅱ中发生Cu与硝酸银的反应,生成硝酸铜和Ag,化学反应为Cu+2AgNO3═Cu(NO3)2+2Ag,观察到现象为红色铜丝上有白色金属Ag附着,
故答案为:红色铜丝上有白色金属Ag附着;Cu+2AgNO3═Cu(NO3)2+2Ag;
(3)由I中反应可知Fe为还原剂,Ⅱ中反应Cu为还原剂,由还原性的还原性大于还原产物的还原性可知,还原性为Fe>Cu>Ag,故答案为:Fe>Cu>Ag.
(2)Ⅱ中发生Cu与硝酸银的反应,生成硝酸铜和Ag,化学反应为Cu+2AgNO3═Cu(NO3)2+2Ag,观察到现象为红色铜丝上有白色金属Ag附着,
故答案为:红色铜丝上有白色金属Ag附着;Cu+2AgNO3═Cu(NO3)2+2Ag;
(3)由I中反应可知Fe为还原剂,Ⅱ中反应Cu为还原剂,由还原性的还原性大于还原产物的还原性可知,还原性为Fe>Cu>Ag,故答案为:Fe>Cu>Ag.
点评:本题考查金属及化合物的性质,为高频考点,把握金属活泼性及氧化还原反应原理为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
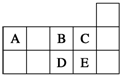 元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )
元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )| A、D在过量的B中燃烧的主要产物为DB3 |
| B、C的氢化物的水溶液酸性比E的强 |
| C、D与B形成的阴离子可能有DB32-、D2B42- |
| D、E单质中由于形成了氢键,所以很容易液化 |
据报道,俄罗斯特种部队在解救人质时除使用了非致命武器芬太奴外,还使用了一种麻醉作用比吗啡强100倍的氟烷.已知氟烷的化学式为C2HClBrF3,则沸点不同的氟烷有( )
| A、1种 | B、2种 | C、3种 | D、4种 |
下面是天津大学化工学院研制的2,6-二氯苯胺的合成路线:下列说法正确的是( )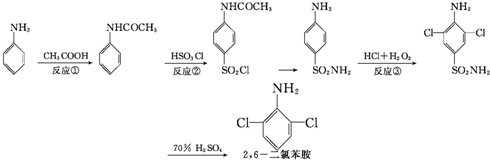

| A、反应①属于取代反应,反应②属于加成反应 |
| B、反应①属于取代反应,反应③属于氧化反应 |
| C、反应①属于取代反应,反应③属于取代反应 |
| D、反应②属于取代反应,反应③属于加成反应 |
配制0.1mol?L-1的CuSO4溶液时,下列情况会导致所配溶液的实际浓度偏高的是( )
| A、定容时仰视容量瓶的刻度线 |
| B、容量瓶没有烘干 |
| C、托盘天平的砝码生锈 |
| D、定容时加水多后用滴管吸出 |
化学已经渗透到人类生活的各个方面,下列说法不正确的是( )
| A、臭氧可用于水体消毒,是因为臭氧能杀死水中的细菌 |
| B、明矾能水解生成氢氧化铝胶体,可用做净水剂 |
| C、食盐中添加碘酸钾,是因为碘酸钾具有氧化性 |
| D、禁止使用四乙基铅作汽油抗暴震剂,可减少汽车尾气污染 |

 工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).下图表示反应中能量的变化.
工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).下图表示反应中能量的变化.