题目内容
实现下列转化的反应方程式中,正确的是( )
| A、Fe→Fe3+:2Fe+6H+═2Fe3++3H2↑ |
| B、H2SO3→H2SO4:2H2SO3+O2═2H2SO4 |
| C、Cu→CuSO4:Cu+2H2SO4(稀)═CuSO4+SO2↑+2H2O |
| D、Br-→Br2:2Br-+I2═Br2+2I- |
考点:铁的化学性质,氯、溴、碘及其化合物的综合应用,浓硫酸的性质,含硫物质的性质及综合应用
专题:元素及其化合物
分析:A、铁和非氧化性酸的反应生成亚铁盐和氢气;
B、亚硫酸具有还原性,能被氧化为硫酸;
C、金属铜可以和浓硫酸之间反应,但是和稀硫酸之间不反应;
D、溴离子具有还原性,能被氧化剂氧化为溴单质.
B、亚硫酸具有还原性,能被氧化为硫酸;
C、金属铜可以和浓硫酸之间反应,但是和稀硫酸之间不反应;
D、溴离子具有还原性,能被氧化剂氧化为溴单质.
解答:
解:A、金属铁可以和强氧化剂反应生成三价铁离子,但是铁和非氧化性酸的反应生成亚铁盐和氢气,即Fe+2H+═Fe2++H2↑,故A错误;
B、亚硫酸具有还原性,能被氧气氧化为硫酸,故B正确;
C、Cu可以和浓硫酸之间发生反应生成硫酸铜,但是Cu和2H2SO4(稀)之间不会发生反应,故C错误;
D、溴离子具有还原性,能被氧化剂氧化为溴单质,但是碘单质的氧化性比溴单质的弱,所以2Br-+I2═Br2+2I-不能发生,故D错误.
故选B.
B、亚硫酸具有还原性,能被氧气氧化为硫酸,故B正确;
C、Cu可以和浓硫酸之间发生反应生成硫酸铜,但是Cu和2H2SO4(稀)之间不会发生反应,故C错误;
D、溴离子具有还原性,能被氧化剂氧化为溴单质,但是碘单质的氧化性比溴单质的弱,所以2Br-+I2═Br2+2I-不能发生,故D错误.
故选B.
点评:本题考查了离子方程式、化学方程式书写方法和正误判断,物质性质和反应实质是解题关键,题目较简单.

练习册系列答案
相关题目
有关化学用语正确的是( )
| A、乙烯的最简式C2H4 |
| B、乙醛的结构简式C2H4O |
C、四氯化碳的电子式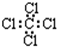 |
| D、乙酸乙酯的分子式C4H8O2 |
下列说法不正确的是( )
| A、石油分馏得到汽油、煤油和柴油是化学变化 |
| B、乙烯和苯是来自石油和煤的两种有机物,它们都能发生加成反应 |
| C、石油裂解得到乙烯、丙烯、丁二烯 |
| D、“西气东输”就是将新疆等地的天然气通过管道输到长江三角洲 |
下列物质中属于非电解质的是( )
| A、硫酸铜 | B、HCl |
| C、NaOH | D、蔗糖 |
下列各组名词或现象中,三者间没有逐级因果关系的是( )
| A、含汞废水----------重金属污染-------------------水俣病患者 |
| B、含磷洗衣粉-------水体富营养化----------------水栖生物死亡 |
| C、石油泄漏----------原油污染-----------------海洋生物死亡 |
| D、二氧化碳----------室内空气污染---------------缺氧中毒 |
几种微粒,具有相同的质子数,则可说明( )
| A、一定是同一种元素 |
| B、可能属于同一种元素 |
| C、一定不是同一种元素 |
| D、核外电子个数一定相等 |
某元素原子R的质量数为A,Rm-的核外电子数为x,则Wg Rm-离子所含中子的物质的量为( )
| A、(A-x+m) mol | ||
| B、(A-x-m) mol | ||
C、
| ||
D、
|
下列卤代烃中,能发生消去反应的是( )
| A、CH3Cl |
| B、CH3CH2-C(CH3)2CH2Br |
| C、CH3CH2-C(CH3)2Cl |
| D、CH2Br-CH(CH3)2 |
下列离子或分子能够在指定的分散系中大量共存的是( )
A、c(H+)=
| ||
| B、苯酚钠溶液中:HCO3-、Na+、K+、CH3COO- | ||
| C、铁与稀硫酸反应制取H2后的溶液中:K+、AlO2-、SO42-、Br- | ||
| D、新鲜的空气:SO2、NO、N2、NH3 |