题目内容
有一种蓝色的晶体,它的结构特征是Fe2+和Fe3+分别占据立方体互不相邻的顶点,立方体的每条棱上均有一个CN-.
(1)根据晶体结构的特点,推出这种蓝色晶体的化学式(用简单整数表示) .
(2)此化学式带何种电荷 ,如用Rn+或Rn-与其结合成电中性粒子,此粒子的化学式为 .
(1)根据晶体结构的特点,推出这种蓝色晶体的化学式(用简单整数表示)
(2)此化学式带何种电荷
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:(1)利用均摊法计算含有的各种离子个数,从而确定其化学式;
(2)根据正负化合价的代数和判断带何种电荷,用带相反电荷的离子结合呈电中性的物质,根据化合价的代数和为0确定M离子的个数,从而写出其化学式;
(2)根据正负化合价的代数和判断带何种电荷,用带相反电荷的离子结合呈电中性的物质,根据化合价的代数和为0确定M离子的个数,从而写出其化学式;
解答:
解:(1)亚铁离子个数=4×
,铁离子个数=4×
,CN-离子个数=12×
=3,所以其化学式为:[FeFe(CN)6]-,
故答案为:[FeFe(CN)6]-;
(2)根据(1)知,该离子带负电荷,用带正电荷的离子可与其结合成电中性的物质,根据化合物中化合价的代数和为0知,Rn+应该是一个正电荷,所以其化学式为R[FeFe(CN)6],
故答案为:负电荷;R[FeFe(CN)6].
| 1 |
| 8 |
| 1 |
| 8 |
| 1 |
| 4 |
故答案为:[FeFe(CN)6]-;
(2)根据(1)知,该离子带负电荷,用带正电荷的离子可与其结合成电中性的物质,根据化合物中化合价的代数和为0知,Rn+应该是一个正电荷,所以其化学式为R[FeFe(CN)6],
故答案为:负电荷;R[FeFe(CN)6].
点评:本题考查了晶胞的有关计算,明确利用均摊法计算含有的各种离子个数,从而确定其化学式是解本题关键,难度中等.

练习册系列答案
相关题目

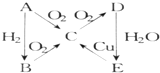 如图所示A、B、C、D、E五种种物质的相互转化关系:
如图所示A、B、C、D、E五种种物质的相互转化关系: 如图所示:若关闭Ⅰ阀,打开Ⅱ阀,让一种含氯气的气体经过甲瓶后,通入乙瓶,布条不褪色;若关闭Ⅱ阀,打开Ⅰ阀再通入这种气体,布条褪色.甲瓶中所盛的试剂可能是( )
如图所示:若关闭Ⅰ阀,打开Ⅱ阀,让一种含氯气的气体经过甲瓶后,通入乙瓶,布条不褪色;若关闭Ⅱ阀,打开Ⅰ阀再通入这种气体,布条褪色.甲瓶中所盛的试剂可能是( )