题目内容
设nA是阿伏加德罗常数的数值。下列说法正确的是
A.1L 0.1mol·L-1的FeCl3溶液中,Fe3+的数目为0.1nA
B.1molNH3中含有N-H键的数目为3nA
C.7.8g Na2O2中含有的阳离子数目为0.1nA
D.标准状况下,22.4L水中分子个数为nA
B
【解析】
试题分析:A、铁离子在溶液中水解,溶液显酸性,因此1L 0.1mol·L-1的FeCl3溶液中,Fe3+的数目小于0.1nA,A错误;B、氨气分子中含有3个N-H键,因此1molNH3中含有N-H键的数目为3nA,B正确;C、过氧化钠的电子式为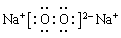 ,7.8g Na2O2的物质的量是0.1mol,其中含有的阳离子数目为0.2nA,C错误;D、标准状况下水不是气态,不能适用于气体摩尔体积,因此22.4L水中分子个数不是nA,D错误,答案选B。
,7.8g Na2O2的物质的量是0.1mol,其中含有的阳离子数目为0.2nA,C错误;D、标准状况下水不是气态,不能适用于气体摩尔体积,因此22.4L水中分子个数不是nA,D错误,答案选B。
考点:考查阿伏伽德罗常数的计算

 快乐小博士巩固与提高系列答案
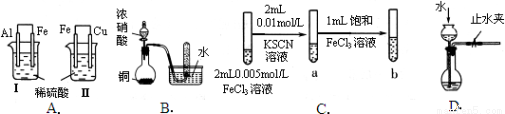
快乐小博士巩固与提高系列答案根据下列实验现象,所得结论错误的是
实验 | 实验现象 | 结论 |
A | Ⅰ烧杯中铁片表面有气泡,Ⅱ烧杯中铜片表面有气泡 | 活动性:Al>Fe>Cu |
B | 试管中收集到无色气体 | 铜与浓硝酸反应产物是NO |
C | 试管b比试管a中溶液的红色深 | 增大反应物浓度,平衡向正反应方向移动 |
D | 长颈漏斗内液面高于烧瓶内液面且保持不变 | 装置气密性良好 |
T1温度下,反应2SO2(g)+O2(g)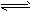 2SO3(g) △H<0的平衡常数K=532.4。
2SO3(g) △H<0的平衡常数K=532.4。
(1)该反应平衡常数的表达式为K= ,T1温度下,某时刻测得体系中各物质浓度分别为c(SO2)=0.0600 mol·L-1,c(O2)=0.400 mol·L-1,c(SO3)=2.000mol·L-1,此时反应进行的方向为 。
(2)该反应△S 0,升高温度,平衡常数 (填“增大”“减小”或“不变”)
(3)T2温度下,2L容积固定的甲、乙两密闭容器中发生上述反应,测得平衡时有关数据如下:
容器 | 甲 | 乙 |
反应物投入量 | 2molSO2、1molO2 | 4molSO3 |
平衡时n(SO3)/mol | 1 | m |
反应物的转化率 | ?1 | ?2 |
①下列能说明T2温度下甲容器中上述反应已达到平衡状态的是 。
A.SO2、O2、SO3的物质的量浓度之比为2:1:2
B.容器内气体压强不再变化
C.单位时间内2v(SO2)消耗= v(O2)生成
D.容器内混合气体的密度不再变化
②分析表格中数据,?1+?2 1(填“>”“=”或“<”),T1 T2(填“>”“=”或“<”)。

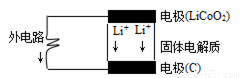
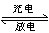 LiCoO2+6C,下列说法错误的是
LiCoO2+6C,下列说法错误的是