题目内容
表是周期表中的一部分,根据A-I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是 ,只有负价而无正价的是 ,氧化性最强的单质是 ,还原性最强的单质是 .
(2)元素的最高价氧化物对应的水化物中,碱性最强的是 ,酸性最强的是 ,呈两性的是 .
(3)A与D、E、F、G、H形成的化合物呈碱性的分子式为 ,最稳定的是 .
(4)在B、C、D、E、F、G、H中,原子半径最大的是 .
| 周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | O |
| 一 | A | |||||||
| 二 | D | E | G | I | ||||
| 三 | B | C | F | H |
(2)元素的最高价氧化物对应的水化物中,碱性最强的是
(3)A与D、E、F、G、H形成的化合物呈碱性的分子式为
(4)在B、C、D、E、F、G、H中,原子半径最大的是
考点:元素周期表的结构及其应用,元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表的位置可知,A为H,B为Na,C为Al,D为C,E为N,F为P,H为S,G为F,I为Ne,
(1)稀有气体性质最不活泼,只有F没有正价,其单质氧化性最强,活泼金属Na的还原性最强;
(2)金属性越强,最高价氧化物对应的水化物碱性越强;非金属性越强,最高价氧化物对应的水化物酸性越强;氢氧化铝为两性化合物;
(3)呈碱性的只有氨气,非金属性越强,气态氢化物越稳定;
(4)电子层越多,半径越大,同周期原子序数最小的原子半径最大.
(1)稀有气体性质最不活泼,只有F没有正价,其单质氧化性最强,活泼金属Na的还原性最强;
(2)金属性越强,最高价氧化物对应的水化物碱性越强;非金属性越强,最高价氧化物对应的水化物酸性越强;氢氧化铝为两性化合物;
(3)呈碱性的只有氨气,非金属性越强,气态氢化物越稳定;
(4)电子层越多,半径越大,同周期原子序数最小的原子半径最大.
解答:
解:由元素在周期表的位置可知,A为H,B为Na,C为Al,D为C,E为N,F为P,H为S,G为F,I为Ne,
(1)化学性质最不活泼的是Ne,只有负价而无正价的是F,氧化性最强的单质是F2,还原性最强的单质是Na,故答案为:Ne;F;F2;Na;
(2)金属性的为Na,最高价氧化物对应的水化物NaOH的碱性最强;非金属性F>N>S,F没有正价,最高价氧化物对应的水化物HNO3的酸性最强;Al(0H)3为两性化合物,故答案为:NaOH;HNO3;Al(0H)3;
(3)呈碱性的只有氨气,分子式为NH3,非金属性最强的为F,则HF最稳定,故答案为:NH3;HF;
(4)电子层越多,半径越大,同周期原子序数最小的原子半径最大,则Na的原子半径最大,故答案为:Na.
(1)化学性质最不活泼的是Ne,只有负价而无正价的是F,氧化性最强的单质是F2,还原性最强的单质是Na,故答案为:Ne;F;F2;Na;
(2)金属性的为Na,最高价氧化物对应的水化物NaOH的碱性最强;非金属性F>N>S,F没有正价,最高价氧化物对应的水化物HNO3的酸性最强;Al(0H)3为两性化合物,故答案为:NaOH;HNO3;Al(0H)3;
(3)呈碱性的只有氨气,分子式为NH3,非金属性最强的为F,则HF最稳定,故答案为:NH3;HF;
(4)电子层越多,半径越大,同周期原子序数最小的原子半径最大,则Na的原子半径最大,故答案为:Na.
点评:本题考查元素周期表的结构及应用,为高频考点,把握元素的位置、性质及应用为解答的关键,注意元素周期律的应用,题目难度不大.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
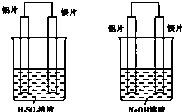 有甲和乙两位同学均想利用原电池反应来检测金属的活动性顺序,两人都使用镁片和铝片作电极,但甲同学将电极放到6mol?L-1 H2SO4溶液中,乙同学将电极放到6mol?L-1NaOH溶液中,如图所示:
有甲和乙两位同学均想利用原电池反应来检测金属的活动性顺序,两人都使用镁片和铝片作电极,但甲同学将电极放到6mol?L-1 H2SO4溶液中,乙同学将电极放到6mol?L-1NaOH溶液中,如图所示: