题目内容
某化工厂为了综合利用生产过程中的副产品CaSO4,与相邻的合成氨厂联合设计了以下制备(NH4)2SO4的工艺流程:

试填空:
(1)沉淀池中发生主要反应的化学方程式为: ,该反应能够发生的原因是: .
(2)提纯滤液以获得(NH4)2SO4晶体,必要的操作步骤是: (填序号).
A.萃取B.蒸发浓缩C.冷却结晶D.蒸馏
(3)该生产过程中可以循环使用的物质X是: (填化学式).
(4)上述生产流程中,有关NH3的作用及说明正确的是: (填序号).
A.提供制备所需的氮元素 B.增大CO32-的浓度促进反应发生
C.作反应的催化剂 D.生产1mol (NH4)2SO4,至少消耗2mol NH3.

试填空:
(1)沉淀池中发生主要反应的化学方程式为:
(2)提纯滤液以获得(NH4)2SO4晶体,必要的操作步骤是:
A.萃取B.蒸发浓缩C.冷却结晶D.蒸馏
(3)该生产过程中可以循环使用的物质X是:
(4)上述生产流程中,有关NH3的作用及说明正确的是:
A.提供制备所需的氮元素 B.增大CO32-的浓度促进反应发生
C.作反应的催化剂 D.生产1mol (NH4)2SO4,至少消耗2mol NH3.
考点:副产品的综合利用,氨的用途,含硫物质的性质及综合应用
专题:氧族元素,氮族元素
分析:(1)根据反应物推测生成物,不难发现生成的沉淀为CaCO3;利用沉淀溶解平衡原理进行分析;
(2)获得晶体,应先浓缩溶液,再进行冷却结晶,从而得到晶体;
(3)根据工艺流程图可知,在煅烧炉中进行煅烧的物质中含有,CaCO3可得到CO2,据此判断;
(4)NH3可以促进吸收CO2,而本身被转化为(NH4)2SO4晶体,据此分析选项.
(2)获得晶体,应先浓缩溶液,再进行冷却结晶,从而得到晶体;
(3)根据工艺流程图可知,在煅烧炉中进行煅烧的物质中含有,CaCO3可得到CO2,据此判断;
(4)NH3可以促进吸收CO2,而本身被转化为(NH4)2SO4晶体,据此分析选项.
解答:
解:(1)将NH3和CO2通入沉淀池中并加入CaSO4,生成(NH4)2SO4和CaCO3,发生CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4,
故答案为:CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4;
(2)从溶液中获取晶体应采取蒸发浓缩、冷却结晶等操作,所以必须操作步骤是BC,
故答案为:BC;
(3)由工艺流程可知,CaCO3在煅烧炉中分解生成CO2和CaO,CO2循环使用,
故答案为:CO2.
(4)A、NH3被转化为(NH4)2SO4晶体,提供了所需要的氮元素,故A正确;
B、氨气可以与CO2反应,促进CO2转化为CO32-,而增大CO32-的浓度,故B正确;
C、氨气参与反应,其物质的量减少,不做催化剂,故C错误;
D、根据化学方程式可知,生产1mol (NH4)2SO4,至少消耗2mol NH3,故D正确;
故选:ABD.
故答案为:CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4;
(2)从溶液中获取晶体应采取蒸发浓缩、冷却结晶等操作,所以必须操作步骤是BC,
故答案为:BC;
(3)由工艺流程可知,CaCO3在煅烧炉中分解生成CO2和CaO,CO2循环使用,
故答案为:CO2.
(4)A、NH3被转化为(NH4)2SO4晶体,提供了所需要的氮元素,故A正确;
B、氨气可以与CO2反应,促进CO2转化为CO32-,而增大CO32-的浓度,故B正确;
C、氨气参与反应,其物质的量减少,不做催化剂,故C错误;
D、根据化学方程式可知,生产1mol (NH4)2SO4,至少消耗2mol NH3,故D正确;
故选:ABD.
点评:本题考查化学工艺流程,应能够结合生产实际,来分析该题,难度不大,其中关于氨气的作用是难点.

练习册系列答案
相关题目
检验某未知溶液中是否含有氯离子,正确的操作是( )
| A、向未知溶液中加入硝酸银溶液,有白色沉淀产生 |
| B、向未知溶液中加入硝酸银溶液,有白色沉淀产生,加入盐酸后.沉淀不消失 |
| C、向未知溶液中加入稀硝酸酸化后,再加入硝酸银溶液,有白色沉淀产生 |
| D、向未知溶液中加入稀盐酸酸化后,再加入硝酸银溶液,有白色沉淀产生 |
下列叙述正确的是( )
| A、检验CO2与Na2O2反应有O2生成,可将CO2气体依次通过Na2O2和浓NaOH溶液,然后收集并用带火星的木条验证 |
| B、除CO2中混有的少量SO2,可依次通过盛有酸性KMnO4溶液、品红溶液的洗气瓶,得纯净CO2 |
| C、检验Fe3O4中混有Fe2O3,可将混合物加入足量稀硫酸溶液,然后取样加入KSCN溶液 |
| D、检验Cl2中混有SO2,可将混合气体通入品红溶液 |
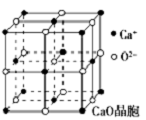 可以由下列反应合成三聚氰胺:CaO+3C
可以由下列反应合成三聚氰胺:CaO+3C )俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸 (
)俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸 (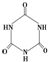 )后,三聚氰酸与三聚氰胺分子相互之间通过
)后,三聚氰酸与三聚氰胺分子相互之间通过 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、醋酸,D中放有饱和碳酸钠溶液.请回答:
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、醋酸,D中放有饱和碳酸钠溶液.请回答: