题目内容
3.决定气体体积的主要微观因素是( )| A. | 气体分子的数目和分子本身的大小 | |
| B. | 气体分子的质量和分子本身的大小 | |
| C. | 气体分子本身的大小和分子间的平均距离 | |
| D. | 气体分子的数目和分子间的平均距离 |
分析 影响物质体积的微观因素有1、分子间的平均距离,2、分子的数目,3、分子本身的大小;而气体分子之间的平均距离远大于气体分子本身的大小,据此分析.
解答 解:影响物质体积的微观因素有1、分子间的平均距离,2、分子的数目,3、分子本身的大小;由于气体分子之间的平均距离远大于气体分子本身的大小,所以决定气体体积的主要微观因素是气体分子的数目和分子间的平均距离.故选D.
点评 本题考查决定气体体积的主要微观因素,难度不大.要注意气体分子之间的平均距离远大于气体分子本身的大小.

练习册系列答案
相关题目
8.下列物质中,不属于卤代烃的是( )
| A. | 氯乙烯 | B. | 溴苯 | C. | 四氯乙烯 | D. | 二氧化硅 |
11.设NA为阿伏加德罗常数,下列叙述中不正确的是( )
| A. | 46g NO2和N2O4混合气体中含有原子数为3NA | |
| B. | 1mol Na2O2和Na2O中离子总数均为2NA | |
| C. | 1mol Mg与足量O2或N2反应均失去2NA个电子 | |
| D. | 标准状况下22.4L H2含有NA个分子 |
18.ClO2是一种杀菌消毒效率高、二次污染小的水处理剂.实验室中可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2ClO2↑+K2SO4+2CO2↑+2H2O. 下列说法不正确的是( )
| A. | 1mol KClO3参加反应,转移2mol电子 | |
| B. | KClO3在反应中被还原 | |
| C. | H2C2O4的还原性强于ClO2 | |
| D. | CO2是H2C2O4被氧化后得到的产物 |
8.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA | |
| B. | 标准状况下,2.24L NO和2.24L O2混合后气体分子数为0.15 NA | |
| C. | 加热条件下,1mol Fe投入足量的浓硫酸中,生成NA个SO2分子 | |
| D. | 0.1mol Na2O2与足是的潮湿的二氧化碳反应转移的电子数为0.1NA |
15.X、Y、Z、M、Q是中学化学常见的五种元素,原子序数依次增大,其结构或性质信息如表:
(1)Q元素基态原子的电子排布式是:1s22s22p63s23p63d64s2.比Q元素原子序数大3的元素的原子结构示意图为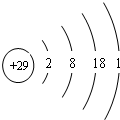 .
.
(2)比较Y元素与氧元素的第一电离能大小顺序N>O;X和Z形成的化合物XZ2为一种液体溶剂,其电子式为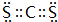 .
.
(3)写出实验室制备M单质的离子方程式:MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++2H2O.
(4)M的气态氢化物和氟化氢相比稳定性强的是HF>HCl (写化学式):
| 元素 | 结构或性质信息 |
| X | 其原子最外层电子数是内层电子数的2倍 |
| Y | 基态原子最外层电子排布为nsnnpn+1 |
| Z | 非金属元素,其单质为固体,在氧气中燃烧时有明亮的蓝紫色火焰 |
| M | 单质在常温、常压下是气体.基态原子的M层上有1个未成对的p电子 |
| Q | 其与X形成的合金为目前用量最多的金属材料 |
 .
.(2)比较Y元素与氧元素的第一电离能大小顺序N>O;X和Z形成的化合物XZ2为一种液体溶剂,其电子式为
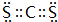 .
.(3)写出实验室制备M单质的离子方程式:MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++2H2O.
(4)M的气态氢化物和氟化氢相比稳定性强的是HF>HCl (写化学式):
13.下列叙述不正确的是( )
| A. | 工业上电解饱和食盐水的阳极反应为:2Cl--2e-═Cl2↑ | |
| B. | 船底镶嵌锌块,锌作负极,以防船体被腐蚀 | |
| C. | 钢铁吸氧腐蚀的正极反应为:O2+2H2O+4e-═4OH- | |
| D. | 铁表面镀锌,铁作阳极 |

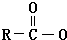 Na+NaOH$→_{△}^{CaO}$R-H+Na2CO3
Na+NaOH$→_{△}^{CaO}$R-H+Na2CO3 ,K的结构简式为
,K的结构简式为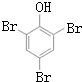 .
.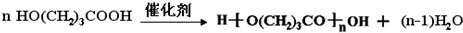 ;
;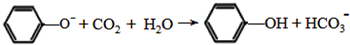 .
. (写结构简式).
(写结构简式).