题目内容
10.已知反应A(s)+B(g)?C(g)+D(g)的化学平衡常数和温度的关系如表:| 温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| 化学平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
| A. | 该反应为吸热反应 | |
| B. | 该反应的化学平衡常数表达式为K=$\frac{c(C)•c(D)}{c(A)•c(B)}$ | |
| C. | 其他条件不变时,增大体系的压强,化学平衡常数减小 | |
| D. | 单位时间内生成B和D的物质的量相等时,该反应处于平衡状态 |
分析 A.升高温度,平衡向吸热方向移动;
B.化学平衡常数K等于生成物浓度幂之积与反应物幂之积的比(但固体和纯液体除外);
C.化学平衡常数只与温度有关;
D.可逆反应达到平衡状态时,同一物质的正逆反应速率相等.
解答 解:A.升高温度,平衡向吸热方向移动,根据表中数据知,升高温度平衡常数减小,说明平衡逆向移动,则正反应是放热反应,故A错误;
B.化学平衡常数K等于生成物浓度幂之积与反应物幂之积的比(但固体和纯液体除外),所以该反应的化学平衡常数K=$\frac{c(C).c(D)}{c(B)}$,故B错误;
C.化学平衡常数只与温度有关,与压强无关,所以他条件不变时,增大体系的压强,化学平衡常数不变,故C错误;
D.可逆反应达到平衡状态时,同一物质的正逆反应速率相等,单位时间内生成B和D的物质的量相等时,同时消耗B和生成B的物质的量相等,则该反应处于平衡状态,故D正确;
故选D.
点评 本题考查化学平衡常数有关问题、化学平衡状态判断等知识点,为高频考点,侧重考查学生分析判断及理解能力,明确化学平衡状态判断方法、化学平衡常数表达式及含义是解本题关键,注意化学平衡常数与压强、浓度、催化剂等都无关系,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.(Ⅰ)氨基甲酸铵(NH2COONH4)的制备氨基甲酸铵是一种白色固体,易分解、易水解,难溶于CCl4.可用做肥料.
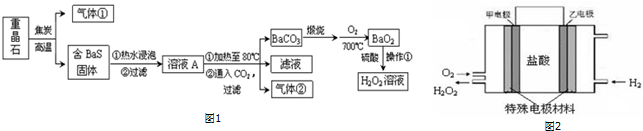
制备氨基甲酸铵的装置如图1所示.反应的化学方程式如下:2NH3(g)+CO2(g)?NH2COONH4(s)△H<0.

注:四氯化碳与液体石蜡均为惰性介质.
(1)发生器用冰水冷却的原因是降低温度,防止因反应放热造成产物分解.提高反应物转化率.
(2)液体石蜡鼓泡瓶的作用是通过观察气泡,调节NH3与CO2通入比例.
(3)从反应后的混合物中分离出产品的实验方法是过滤(填写操作名称).为了得到干燥产品,应采取的方法是c(填写选项序号).
a.80℃热风下烘干 b.60℃热风下烘干 c.40℃热风下烘干
(4)尾气处理装置如图2所示.双通玻璃管的作用:防止倒吸;
浓硫酸的作用:吸收多余氨气、防止空气中水蒸气进入反应器使氨基甲酸铵水解.
(5)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000g.则样品中氨基甲酸铵的物质的量分数为80%.(精确到2位小数,碳酸氢铵和氨基甲酸铵的相对分子质量分别为79和78)
(Ⅱ) FeSO4•7H2O晶体的制备
(6)已知:
某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)出发,制备绿矾(FeSO4•7H2O),补充完整由硫铁矿烧渣制备FeSO4•7H2O晶体的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):
①向一定量烧渣中加入足量的稀硫酸充分反应,充分反应后过滤,
②向滤液加入足量的铁粉,充分搅拌后,过滤,
③滤液中滴加NaOH溶液调节反应液的pH约为5.0~5.8,过滤,
④将得到溶液加热蒸发浓缩,冷却结晶,过滤,洗涤,低温干燥,得到FeSO4•7H2O晶体.
制备氨基甲酸铵的装置如图1所示.反应的化学方程式如下:2NH3(g)+CO2(g)?NH2COONH4(s)△H<0.

注:四氯化碳与液体石蜡均为惰性介质.
(1)发生器用冰水冷却的原因是降低温度,防止因反应放热造成产物分解.提高反应物转化率.
(2)液体石蜡鼓泡瓶的作用是通过观察气泡,调节NH3与CO2通入比例.
(3)从反应后的混合物中分离出产品的实验方法是过滤(填写操作名称).为了得到干燥产品,应采取的方法是c(填写选项序号).
a.80℃热风下烘干 b.60℃热风下烘干 c.40℃热风下烘干
(4)尾气处理装置如图2所示.双通玻璃管的作用:防止倒吸;
浓硫酸的作用:吸收多余氨气、防止空气中水蒸气进入反应器使氨基甲酸铵水解.
(5)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000g.则样品中氨基甲酸铵的物质的量分数为80%.(精确到2位小数,碳酸氢铵和氨基甲酸铵的相对分子质量分别为79和78)
(Ⅱ) FeSO4•7H2O晶体的制备
(6)已知:
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
①向一定量烧渣中加入足量的稀硫酸充分反应,充分反应后过滤,
②向滤液加入足量的铁粉,充分搅拌后,过滤,
③滤液中滴加NaOH溶液调节反应液的pH约为5.0~5.8,过滤,
④将得到溶液加热蒸发浓缩,冷却结晶,过滤,洗涤,低温干燥,得到FeSO4•7H2O晶体.
1.下列有关物质的分类正确的是( )
| A. | 纯净物:水银、氢氧化铁固体、冰水混合物 | |
| B. | 碱性氧化物:Na2O、Na2O2、Al2O3 | |
| C. | 盐:纯碱、小苏打、烧碱 | |
| D. | 电解质:CH3COOH、H2O、NH3 |
5.氮氧化铝(AlON)属原子晶体,是一种超强透明材料,可以由反应Al2O3+C+N2$\frac{\underline{\;\;△\;\;}}{\;}$2AlON+CO合成,下列有关说法正确的是( )
| A. | 氮氧化铝中氮的化合价是-3 | |
| B. | 反应中氧化产物和还原产物的物质的量之比是1:2 | |
| C. | 反应中每生成5.7gAlON同时生成1.12LCO | |
| D. | AlON和CO的化学键类型不同 |
15.X、Y、Z、W均为短周期主族元素,且原子序数逐渐增大.已知:
①X、Y、W分别位于不同周期;
②Z和W属于同一主族,且W的原子序数是Z的两倍;
③Y、Z、W的最外层电子数之和为17.
下列说法不正确的是( )
①X、Y、W分别位于不同周期;
②Z和W属于同一主族,且W的原子序数是Z的两倍;
③Y、Z、W的最外层电子数之和为17.
下列说法不正确的是( )
| A. | 原子半径由小到大的顺序为r(X)<r(Y)<r(Z)<r(W) | |
| B. | X、Y、Z既能形成离子化合物,又能形成共价化合物 | |
| C. | Z分别能与X、Y和W形成多种化合物 | |
| D. | 与单质W比较,单质Z更容易与单质X化合 |
16.常温下H2S饱和溶液1L,其浓度为0.1mol/L,电离方程式为H2S?H++HS-,HS-?H++S2-若要使溶液中的pH值增大同时使c(S2-)减小,可采取的措施是( )
| A. | 加入适量水 | B. | 加入适量NaOH固体 | ||
| C. | 通入适量的O2 | D. | 加入适量的CuSO4 |