题目内容
19.在密闭容器中发生如下反应:aX(g)+bY(g)?cZ(g)+dW(g),反应达平衡后保持温度不变,将气体体积压缩到原来的一半,当再次达平衡时,W的浓度为原平衡时的1.85倍.下列叙述中错误的是( )| A. | 平衡向逆反应方向移动 | B. | a+b<c+d | ||
| C. | Z的体积分数增加 | D. | X的转化率提高 |
分析 aX(g)+bY(g)?cZ(g)+dW(g),反应达平衡后保持温度不变,将气体体积压缩到原来的一半,如果平衡不移动,则W浓度应该是原来的2倍,实际上当再次达平衡时,W的浓度为原平衡时的1.85倍,说明增大压强平衡逆向移动,据此分析解答.
解答 解:aX(g)+bY(g)?cZ(g)+dW(g),反应达平衡后保持温度不变,将气体体积压缩到原来的一半,如果平衡不移动,则W浓度应该是原来的2倍,实际上当再次达平衡时,W的浓度为原平衡时的1.85倍,说明增大压强平衡逆向移动,
A.通过以上分析知,平衡逆向移动,故A正确;
B.增大压强平衡向气体体积减小的方向移动,所以a+b<c+d,故B正确;
C.平衡逆向移动,Z的物质的量减小,Z的体积分数降低,故C错误;
D.平衡逆向移动,X的转化率降低,故D错误;
故选CD.
点评 本题考查化学平衡移动原理,为高频考点,侧重考查学生分析判断能力,正确建立假设是解本题关键,很多同学往往单纯根据W浓度判断反应方向而导致错误,为易错题.

练习册系列答案
相关题目
10.下列说法正确的是( )
| A. | 已知:Ⅰ:对于反应:H2(g)+Cl2(s)═2HCl (g)△H=-a kJ/mol, Ⅱ:  且a、b、c均大于零,则断开1molH-Cl键所需的能量为-a-b-c | |
| B. | 若2C(s)+O2(g)═2CO(g)△H=-221.0 kJ/mol,则碳的燃烧热为110.5 kJ/mol | |
| C. | 需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 | |
| D. | 如图可表示水分解过程中的能量变化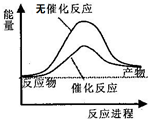 |
7.在一个盛有催化剂容积可变的密闭容器中,保持一定的温度和压强,进行以下反应:N2+3H2?2NH3.已知加入1molN2和4molH2时,达到平衡后生成amolNH3.有恒温恒压下欲保持平衡时各组分的体积分数不变.填表(恒温恒压)
| 已知 编号 | 起始状态物质的量/mol | 平衡时NH3的 物质的量/mol | ||
| N2 | H2 | NH3 | ||
| 1 | 4 | 0 | a | |
| ① | 1.5 | 9 | 0 | >1.5a |
| ② | 0 | 0.5 | 1 | 0.5a |
| ③ | m | g(g≥4m) | 0 | am或者$\frac{ag}{4}$ |
14.同温同压下,下列各组热化学方程式中,△H1<△H2的是( )
| A. | C(s)+$\frac{1}{2}$O2(g)=CO(g);△H1 C(s)+O2(g)=CO2(g);△H2 | |
| B. | $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)=HCl(g);△H1 H2(g)+Cl2(g)=2HCl(g);△H2 | |
| C. | S(g)+O2(g)=SO2(g);△H1 S(s)+O2(g)=SO2(g);△H2 | |
| D. | 2H2(g)+O2(g)=2H2O(g);△H1 2H2(g)+O2(g)=2H2O(l);△H2 |
11.(1)若某药品质量约为32.0g,托盘天平准确称其质量,若用↓表示在右盘放上砝码,用↑表示将砝码取下,在下列表格的空格内,用↓和↑表示相应砝码的放上或取下.
(2)配制500mL 0.1mol•L-1 Na2CO3溶液,图中操作②中应该填写的数据为5.3,实验操作的先后顺序为②④③⑤①⑥ (填编号).
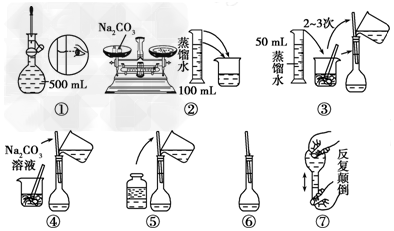
(3)在配制一定物质的量浓度的溶液时,用“偏高、偏低、无影响”表示下列操作对所配溶液浓度的影响.
①用量筒取液态溶质,读数时,俯视量筒,所配制溶液的浓度偏低
②将量取液态溶质的量筒用水洗涤,洗涤液倒入容量瓶,所配制溶液的浓度偏高
③定容摇匀后,有少量溶液外流,对所配制溶液的浓度无影响.
| 50g | 20g | 20g | 10g | 5g |

(3)在配制一定物质的量浓度的溶液时,用“偏高、偏低、无影响”表示下列操作对所配溶液浓度的影响.
①用量筒取液态溶质,读数时,俯视量筒,所配制溶液的浓度偏低
②将量取液态溶质的量筒用水洗涤,洗涤液倒入容量瓶,所配制溶液的浓度偏高
③定容摇匀后,有少量溶液外流,对所配制溶液的浓度无影响.
8.相同温度下,体积相同的两个容器中,充入等质量CO2和CO气体,下列判断正确的是( )
| A. | CO2和CO对容器产生的压强之比是7:11 | |
| B. | CO2和CO的密度之比是11:7 | |
| C. | CO2和CO的分子数相等 | |
| D. | CO2和CO的氧原子个数比是22:7 |
9.已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O.每有1mol Cu(IO3)2参加反应时( )
| A. | 有12 mol KI 被氧化 | B. | 转移11 mol电子 | ||
| C. | 生成CuI 382g | D. | I2只是氧化产物 |