题目内容
3.物质制备过程中离不开物质的提纯. 以下除杂方法正确的是( )| 选项 | 目的 | 试验方法 |
| A | 除去Na2CO3固体中的NaHCO3 | 置于蒸发皿中加热至恒重 |
| B | 除去NaCl中少量KNO3 | 将混合物制成热饱和溶液,冷却结晶,过滤 |
| C | 除去CO2中的HCl | 通过NaHCO3(aq,饱和),然后干燥 |
| D | 除去C2H5Br中的Br2 | 加入足量Na2SO3(aq),充分振荡,蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.加热固体应在坩埚中进行;
B.硝酸钾溶解度受温度影响很大,氯化钠溶解度受温度影响不大;
C.CO2不溶于饱和碳酸氢钠溶液;
D.反应后溶液分层,可用分液的方法分离.
解答 解:A.NaHCO3不稳定,加热易分解,将固体置于坩埚中加热至恒重,可得到纯净的碳酸钠固体,故A错误;
B.硝酸钾溶解度受温度影响很大,氯化钠溶解度受温度影响不大,冷却结晶,氯化钠残留在母液中,且混有硝酸钾,不能得到纯净的氯化钠,应用蒸发结晶的方法,故B错误;
C.二氧化碳与饱和碳酸氢钠溶液不反应,盐酸与碳酸氢钠反应生成二氧化碳气体,可除去杂质,故C正确;
D.Br2可与Na2SO3发生氧化还原反应而被除去,然后分液可得溴乙烷,故D错误.
故选C.
点评 本题考查物质的分离、提纯的实验设计,侧重于学生的分析能力、实验能力的考查,为高频考点,注意把握物质的性质的异同,易错点为B,注意除杂时不能引入新的杂质.

练习册系列答案
相关题目
13.下列说法中正确的是( )
| A. | 反应物的总能量大于生成物的总能量时,△H>0 | |
| B. | △H>0表示放热反应,△H<0表示吸热反应 | |
| C. | △H的大小与热化学方程式中的各物质的化学计量数无关 | |
| D. | 在化学反应中,发生物质变化的同时一定发生能量变化 |
14.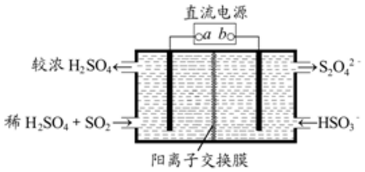 利用如图所示装置(电极均为惰性电极)可吸收SO2,并用阴极排出的溶液可吸收NO2.下列说法正确的是( )
利用如图所示装置(电极均为惰性电极)可吸收SO2,并用阴极排出的溶液可吸收NO2.下列说法正确的是( )
 利用如图所示装置(电极均为惰性电极)可吸收SO2,并用阴极排出的溶液可吸收NO2.下列说法正确的是( )
利用如图所示装置(电极均为惰性电极)可吸收SO2,并用阴极排出的溶液可吸收NO2.下列说法正确的是( )| A. | a为直流电源的负极 | |
| B. | 与 b电极相连的电极反应式为:2HSO3-+2H++2e-═S2O42-+2H2O | |
| C. | 与 a相连的电极发生还原反应得到SO42- | |
| D. | 电解时,H+由阴极室通过阳离子交换膜到阳极室 |
11. 乙酸橙花酯兼有橙花和玫瑰花香气,其结构简式如图.关于该有机物的叙述中正确的是
乙酸橙花酯兼有橙花和玫瑰花香气,其结构简式如图.关于该有机物的叙述中正确的是
①在Ni催化条件下1mol该有机物可与3mol H2发生加成;
②该有机物不能发生银镜反应;
③该有机物分子式为C12H22O2;
④该有机物的同分异构体中不可能有酚类;
⑤1mol该有机物水解时只能消耗1mol NaOH( )
 乙酸橙花酯兼有橙花和玫瑰花香气,其结构简式如图.关于该有机物的叙述中正确的是
乙酸橙花酯兼有橙花和玫瑰花香气,其结构简式如图.关于该有机物的叙述中正确的是①在Ni催化条件下1mol该有机物可与3mol H2发生加成;
②该有机物不能发生银镜反应;
③该有机物分子式为C12H22O2;
④该有机物的同分异构体中不可能有酚类;
⑤1mol该有机物水解时只能消耗1mol NaOH( )
| A. | ②④⑤ | B. | ①④⑤ | C. | ②③⑤ | D. | ①②③ |
18.化学与生活密切相关.下列有关说法错误的是( )
| A. | SiO2、MgO熔点高,可用于制作耐高温仪器 | |
| B. | 天然气是可再生清洁能源,可用于工业制盐酸 | |
| C. | 硝酸铵属于氧化剂,严禁用可燃物(如纸袋)包装 | |
| D. | 纤维素属于多糖类物质,但不能作人类的营养物质 |
8.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA | |
| B. | 0.1 mol丙烯酸(CH2=CHCOOH)中含有碳原子的数目为0.2NA | |
| C. | 标准状况下,11.2LCCl4中含有分子的数目为0.5NA | |
| D. | 在2Na2O2+2H2O═4NaOH+O2↑的反应中,每生成0.1 mol氧气,转移电子的数目为0.1NA |
12.化学与社会、生活密切相关,对下列现象或事实的解释正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | 小苏打用作焙制糕点的膨松剂 | Na2CO3溶液呈碱性 |
| B | 明矾可用于净水 | 明矾在水中生成的氢氧化铝胶体有吸附性 |
| C | SiO2用于制造光导纤维 | SiO2有导电性 |
| D | SO2可使溴水褪色 | SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
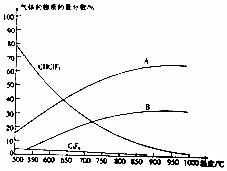 氟的单质及其化合物在生产杀虫剂、灭火剂及特种塑料等方面用途广泛.
氟的单质及其化合物在生产杀虫剂、灭火剂及特种塑料等方面用途广泛. .
. 反应aA(s)+bB(g)?cC(g)+dD(g)达到平衡时,B%跟压强P和温度T(T2>T1)之间的关系如图所示(填“增大”“减小”“吸”“放”“正”“逆”)
反应aA(s)+bB(g)?cC(g)+dD(g)达到平衡时,B%跟压强P和温度T(T2>T1)之间的关系如图所示(填“增大”“减小”“吸”“放”“正”“逆”)