题目内容
将质量分数为30%的硫酸与90%的硫酸等体积混合后,混合液的质量分数为( )
| A、60% | B、>60% |
| C、<60% | D、无法确定 |
考点:溶液中溶质的质量分数及相关计算
专题:物质的量浓度和溶解度专题
分析:令质量分数为30%的硫酸的密度为ρ1g/mL,90%的硫酸的密度为ρ2g/mL,溶液体积为VmL,根据硫酸溶液的浓度愈大,其密度就愈大,则ρ1<ρ2,根据m=ρV表示出两硫酸溶液的质量,进而表示出混合后溶液总质量、溶质硫酸总的质量,再根据ω=
表示出混合后硫酸的质量分数,结合密度关系进行判断.
| m(溶质) |
| m(溶液) |
解答:
解:令质量分数为30%的硫酸的密度为ρ1g/mL,90%的硫酸的密度为ρ2g/mL,溶液体积为VmL,
则混合后溶液的质量为:ρ1g/mL×VmL+ρ2g/mL×VmL=V(ρ1+ρ2)g,
混合后溶质硫酸的总质量为:ρ1g/mL×VmL×30%+ρ2g/mL×VmL×90%=V(30%ρ1+90%ρ2)g,
混合后硫酸的质量分数为:
=
若ρ1=ρ2,混合后所得溶液的溶质质量分数等于60%,硫酸溶液的浓度愈大,其密度就愈大,则ρ1>ρ2,故混合后所得溶液的溶质质量分数大于60%,
故选:B.
则混合后溶液的质量为:ρ1g/mL×VmL+ρ2g/mL×VmL=V(ρ1+ρ2)g,
混合后溶质硫酸的总质量为:ρ1g/mL×VmL×30%+ρ2g/mL×VmL×90%=V(30%ρ1+90%ρ2)g,
混合后硫酸的质量分数为:
| V(30%ρ1+90%ρ2)g |
| V(ρ1+ρ2)g |
| 30%ρ1+90%ρ2 |
| ρ1+ρ2 |
若ρ1=ρ2,混合后所得溶液的溶质质量分数等于60%,硫酸溶液的浓度愈大,其密度就愈大,则ρ1>ρ2,故混合后所得溶液的溶质质量分数大于60%,
故选:B.
点评:本题考主要考查了溶质质量分数的计算,难度中等,清楚硫酸溶液的浓度愈大密度愈大是关键,侧重考查对学生的数据处理能力.

练习册系列答案
相关题目
相同温度下,相同物质的量浓度的七种溶液:①CH3COONa,②NaHSO4,③NaCl,④Na2CO3,⑤NaHCO3,⑥CH3COOH,⑦NH4Cl.按pH 由大到小的顺序排列正确的是( )
| A、⑤④①③⑦⑥② |
| B、②⑥⑦③①⑤④ |
| C、④⑤①③⑦⑥② |
| D、②⑥⑦③①④⑤ |
了解安全知识,可以更好的保护自己.下列做法正确的是( )
| A、用甲醛溶液浸泡水产品以延长保质期 |
| B、在饲料中添加“瘦肉精”以增加猪肉的瘦肉含量 |
| C、高层住房着火.立即打开所有门窗 |
| D、燃着的酒精灯不慎碰到,立即用湿布盖灭 |
如图所示实验设计能达到相应实验目的是( )
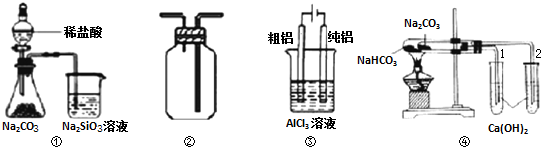

| A、用图①装置验证氯、碳、硅元素非金属性 |
| B、用图②装置能收集O2、CO2和H2 |
| C、用图③装置电解精炼铝 |
| D、用图④装置验证NaHCO3和Na2CO3的热稳定性 |
下列水作为反应物参加的反应中:①钠与水反应 ②Na2O2与水反应 ③氟气与水反应 ④电解水.按照水的作用依次是只作氧化剂、只作还原剂、既作氧化剂又作还原剂、既不作氧化剂又不作还原剂顺序排列是( )
| A、①②③④ | B、①③④② |
| C、①④②③ | D、①④③② |
下列有关0.1mol/LKNO3溶液的叙述正确的是( )
| A、1L该溶液中含KNO3101g | ||
B、100mL该溶液中含N
| ||
| C、从1L该溶液中取出100mL,所取出的KNO3溶液的浓度为0.01mol/L | ||
| D、在1L水中溶解10.1g KNO3,即可配制得0.1mol/L KNO3溶液 |
下列排列顺序正确的是( )
①热稳定性:NH3>HF>H2S
②原子半径:Na>Mg>F
③酸性:H3PO4>H2SO4>HClO4
④结合质子能力:OH->CH3COO->Cl-
⑤晶体的熔点:Si3N4>NaCl>CCl4>SO2
①热稳定性:NH3>HF>H2S
②原子半径:Na>Mg>F
③酸性:H3PO4>H2SO4>HClO4
④结合质子能力:OH->CH3COO->Cl-
⑤晶体的熔点:Si3N4>NaCl>CCl4>SO2
| A、③⑤ | B、①②④ |
| C、全部正确 | D、②④⑤ |
下列物质久置于空气中,颜色发生变化的( )
| A、Na2SO4 |
| B、苯酚 |
| C、Na2O2 |
| D、CaO |
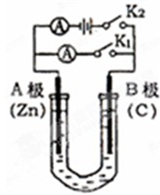 如图所示,U形管内盛有100mL的溶液,请按要求回答下列回答.
如图所示,U形管内盛有100mL的溶液,请按要求回答下列回答.