题目内容
10.0.5体积某气态烃和1体积氯化氢发生加成反应后,最多还能和3体积氯气发生取代反应.由此可以断定原气态烃是( )(气体体积均在相同条件下测定)| A. | 乙炔 | B. | 丙炔 | C. | 丁炔 | D. | 1,3-丁二烯 |
分析 由选项可知,都是链烃,0.5体积某气态烃和与1体积氯气发生加成反应,说明分子中含2个双键或1个C≡C.生成了0.5体积该卤代烷能和3体积氯气发生取代反应,说明1个卤代烷中含有6个H原子,加成时1个烃分子已引入2个H原子形成卤代烷,所以该气体烃分子中含有4个H原子,以此来解答.
解答 解:由选项可知,都是链烃,0.5体积某气态烃和与1体积氯气发生加成反应,说明分子中含2个双键或1个C≡C.生成了0.5体积该卤代烷能和3体积氯气发生取代反应,说明1个卤代烷中含有6个H原子,加成时1个烃分子已引入2个H原子形成卤代烷,所以该气体烃分子中含有4个H原子,
由选项可知,都是链烃,故该气态烃分子中C原子数目为$\frac{4+2}{2}$=3,故ACD错误,B正确,
故选B.
点评 本题考查有机物分子式的确定,难度不大,理解加成反应与取代反应是解题关键.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
1.科学家在研究化学物质吋,常常对物质逬行分类,以便对同类物质的组成和性质进行深人的研究,下列4组物质:
①Ca、S、Cl2、NO2②NH3•H2O、Na2CO3、CH4、KCl③H2CO3、H2SO4、NaOH、H2SiO3④MgO、SO2、CO2、SiO2从物质的基本分类看,每组中都有一种物质与其它物质不属于同这4种物质分别是( )
①Ca、S、Cl2、NO2②NH3•H2O、Na2CO3、CH4、KCl③H2CO3、H2SO4、NaOH、H2SiO3④MgO、SO2、CO2、SiO2从物质的基本分类看,每组中都有一种物质与其它物质不属于同这4种物质分别是( )
| A. | NO2、CH4、NaOH、MgO | B. | Cl2、NH3•H20、NaOH、Si02 | ||
| C. | Ca、Ma2C03、H2Si03、MgO | D. | NO2、CH4、H2SiO3、SO2 |
18.常温下,下列试剂不能用带玻璃塞的试剂瓶盛放的是( )
| A. | 浓盐酸 | B. | 浓硝酸 | C. | 稀盐酸 | D. | 氢氧化钠溶液 |
15.T℃时,A气体与B气体反应生成C气体.反应过程中A、B、C浓度变化如图(1)所示,若保持其他条件不变,温度分别为T1℃和T2℃时,B的体积分数与时间的关系如图(2)所示,则下列结论正确的是( )
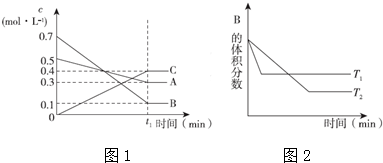

| A. | 该平衡体系的化学反应方程式为:3A(g)+B(g)═4 C(g) | |
| B. | 在t1时间内用B表示该反应的平均速率为0.6/t1mol•L-1•min-1 | |
| C. | 其他条件不变,升高温度,正反应速率减小、逆反应速率增大,A的转化率减小 | |
| D. | 维持温度和容器体积不变,往平衡体系中充惰性气体,C的百分含量增大 |
2.反应A+B═C,在反应过程中,断裂1mol A中的化学键消耗的能量为Q1kJ,断裂1mol B中的化学键消耗的能量为Q2kJ,形成1mol C中的化学键释放的能量为Q3kJ;1mol A所含化学能为E1kJ,1mol B所含化学能E2kJ,1molC 所含化学能E3kJ.下列说法中一定正确的是( )
| A. | 若Q1+Q2<Q3,则反应为放热反应 | B. | 若Q1+Q2>Q3,则反应为放热反应 | ||
| C. | 若E1+E2>E3,则反应为吸热反应 | D. | 若E1+E2>E3,则Q1+Q2>Q3 |
19.有①NaOH溶液②CH3COONa溶液各25mL,物质的量浓度均为0.1mol•L-1,下列说法正确的是( )
| A. | 两种溶液pH的大小顺序是②>① | |
| B. | 若将两种溶液稀释相同倍数,pH变化较大的是② | |
| C. | 若分别加入25mL0.1mol•L-1盐酸后,pH较大的是① | |
| D. | 若两种溶液的pH均为9,则物质的量浓度大小关系是①>② |
20.下列问题与NO2的排放无关的是( )
| A. | 酸雨 | B. | 温室效应 | ||
| C. | 光化学烟雾 | D. | 腐蚀金属和非金属材料 |
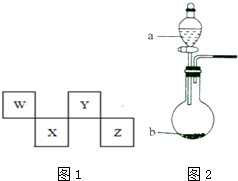 W、X、Y、Z四种短周期元素在周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物.
W、X、Y、Z四种短周期元素在周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物.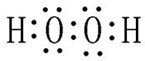 ,Z在周期表中的位置第三周期ⅦA族.
,Z在周期表中的位置第三周期ⅦA族. ;取代反应
;取代反应 ;加成反应
;加成反应 ;取代反应
;取代反应