题目内容
4.向50ml物质的量浓度均为0.1mol/L (NH4)2SO4、Al2(SO4)3溶液中逐滴滴入0.1mol/L Ba(OH)2溶液200ml,随着Ba(OH)2溶液体积的变化,沉淀总物质的量(n)的变化如图所示.下列叙述不正确的是( )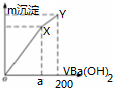
| A. | a=150 | |
| B. | Y点对应溶液为氨水 | |
| C. | OX、XY两段沉淀种类相同 | |
| D. | 继续滴加Ba(OH)2溶液,发生的离子反应为Al(OH)3+OH-═AlO2-+2H2O |
分析 0.1mol/L (NH4)2SO4、Al2(SO4)3溶液中逐滴滴入0.1mol/L Ba(OH)2溶液,首先与硫酸铝反应生成硫酸钡和氢氧化铝沉淀,当硫酸铝完全反应与硫酸铵溶液反应生成一水合铵和硫酸钡,由此分析解答.
解答 解:A、Al2(SO4)3+3Ba(OH)2=BaSO4↓+2Al(OH)3↓,而Al2(SO4)3的物质的量为0.1×50×10-3=5×10-3mol,所以a=$\frac{5×1{0}^{-3}mol}{0.1mol/L}×1{0}^{3}mL/L$=150ml,故A正确;
B、当硫酸铝完全反应与硫酸铵溶液反应生成一水合铵和硫酸钡,所以Y点对应溶液为氨水,故B正确;
C、OX沉淀是硫酸钡和氢氧化铝、XY段沉淀是硫酸钡,所以种类不同,故C错误;
D、继续滴加Ba(OH)2溶液,因为氢氧化铝两性,所以发生Al(OH)3+OH-═AlO2-+2H2O,故D正确;
故选C.
点评 本题考查镁铝化合物性质、混合物的有关计算,难度中等,根据清楚图象反应过程是解题关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列叙述中,正确的是( )
| A. | 含金属元素的离子不一定都是阳离子 | |
| B. | 在氧化还原反应中,非金属单质一定是氧化剂 | |
| C. | 化合物变为单质时,化合价变化的元素一定被还原 | |
| D. | 油锅着火时,立即用水扑灭 |
19.某废水中可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、AlO2一、CO32-、S2一、SO32-、SO42-现取该溶液进行有关实验,实验过程及现象如下:下列说法正确的是( )
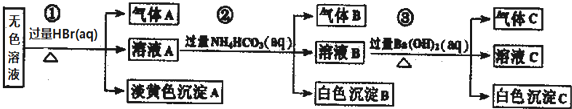

| A. | 根据实验①中的现象可推出,气体A一定是纯净物,淡黄色沉淀一定是AgBr | |
| B. | 根据实验②中的现象可推出,气体B是CO2,沉淀B是Al(OH)3,原溶液中一定含有Al3+ | |
| C. | 根据实验③中的现象可推出,气体C是NH3,沉淀C一定有BaCO3,可能有BaSO4 | |
| D. | 原溶液中肯定含有Na+、AlO2-、S2-,不能确定是否含有SO32-、SO42- |
9.根据你所学习的元素周期律和周期表知识回答下列相关问题:
(1)现有部分短周期元素的性质或原子结构如表:
①元素Y的氢化物的电子式为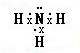 ,其水溶液呈碱性的原因是(用电离方程式表示):NH3•H2O?NH4++OH-.
,其水溶液呈碱性的原因是(用电离方程式表示):NH3•H2O?NH4++OH-.
②元素Z与元素T相比,非金属性较强的是Cl(填元素符号).
③探寻物质的性质差异性是学习的重要方法之一.T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是H2CO3(填化学式).
(2)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质).把与下面元素有关的性质相符的曲线标号填入相应的空格中:

①ⅡA族元素的最外层电子数(填字母)b.
②第三周期元素的最高化合价(填字母)c.
③N3-、O2-、F-、Na+、Mg2+、Al3+的离子半径(填字母)a.
(3)周期表中某些元素化合物的易燃性、毒性变化有一定规律性,例如:
①氢化物的易燃性:第二周期CH4>NH3>H2O>HF;
第三周期SiH4>PH3>H2S>HCl(填化学式).
②化合物的毒性:PH3>NH3,H2S>H2O.CS2>CO2,(选填>、<或=).
(1)现有部分短周期元素的性质或原子结构如表:
| 元素编号 | 元素性质或原子结构 |
| T | 单质是一种淡黄色固体,是黑火药成分之一 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
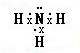 ,其水溶液呈碱性的原因是(用电离方程式表示):NH3•H2O?NH4++OH-.
,其水溶液呈碱性的原因是(用电离方程式表示):NH3•H2O?NH4++OH-.②元素Z与元素T相比,非金属性较强的是Cl(填元素符号).
③探寻物质的性质差异性是学习的重要方法之一.T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是H2CO3(填化学式).
(2)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质).把与下面元素有关的性质相符的曲线标号填入相应的空格中:

①ⅡA族元素的最外层电子数(填字母)b.
②第三周期元素的最高化合价(填字母)c.
③N3-、O2-、F-、Na+、Mg2+、Al3+的离子半径(填字母)a.
(3)周期表中某些元素化合物的易燃性、毒性变化有一定规律性,例如:
①氢化物的易燃性:第二周期CH4>NH3>H2O>HF;
第三周期SiH4>PH3>H2S>HCl(填化学式).
②化合物的毒性:PH3>NH3,H2S>H2O.CS2>CO2,(选填>、<或=).
16.向集满CO2的铝制易拉罐中加入过量NaOH浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起.上述实验过程中没有发生的离子反应是( )
| A. | CO2+2OH-=CO32-+H2O | B. | Al2O3+2OH-=2 AlO2-+H2O | ||
| C. | 2 Al+2OH-+2H2O=2 AlO2-+3H2↑ | D. | Al3++4 OH-=AlO2-+2H2O |
14.下列物质的电子式书写正确的是( )
| A. | 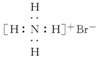 | B. |  | C. |  | D. | 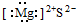 |